Уравнение реакции:
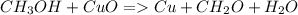
В реакцию вступают пары метилового спирта ![CH_{3}OH[\tex] и оксид меди(II) [tex] CuO [\tex] </p <pВ результате реакции образуются: муравьиный альдегид [tex]CH_{2}O](/tpl/images/0042/0106/8dd15.png) , восстановленная медь
, восстановленная медь 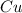 и пары воды
и пары воды 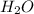
Нам известно:
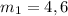 г - масса метилового спирта
г - масса метилового спирта
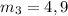 г - масса меди
г - масса меди
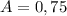 - массовый выход альдегида
- массовый выход альдегида
Найдем молярные массы всех веществ:
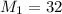 г/моль - молярная масса муравьиного альдегида
г/моль - молярная масса муравьиного альдегида
 г/моль - молярная масса оксида меди (II)
г/моль - молярная масса оксида меди (II)
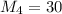 г/моль - молярная масса муравьиного альдегида
г/моль - молярная масса муравьиного альдегида
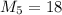 г/моль - молярная масса воды
г/моль - молярная масса воды
Найдем теперь количество метилового спирта в молях:
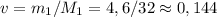 моль
моль
Из уравнения реакции следует, что все оставшиеся вещества надо брать в том же количестве, что метиловый спирт. Найдем неизвестные массы:
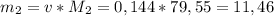 г - масса оксида меди
г - масса оксида меди
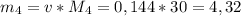 г - теоретическая масса муравьиного альдегида
г - теоретическая масса муравьиного альдегида
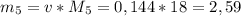 u - масса воды
u - масса воды
Найдем фактическую массу муравьиного альдегида:
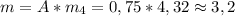
ответ: m=3,2 г
Короче, тут надо знать какой концентрации кислота, ибо реакции при разной концентрации протекают по-разному!
Ладно! Будем думать, что в первом случае у нас фосфорная кислота- безводная, т.е концентрация 100%, тогда составим уравнения реакции:
1)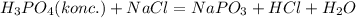 (При не очень высокой температуре)
(При не очень высокой температуре)
2)Пишем в ионной форме: Сразу скажу, поскольку все соли растворимые, и кислоты, то в сокращённой ионной форме получится:
3)Для реакции с магнием, возьмём разбавленную фосфорную кислоту. Если надо реакции с концентрированной, то вот тебе правило: Чем выше концентрация фосфорной кислоты, тем больше атомов металла будут замещаться атомами водорода, т.е будут получаться кислые соли, например: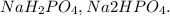
в данном случаем, магний заместил атомы водорода. В ходе данной реакции выпал осадок и выделился газ, запишем это в полной и сокращённой ионных формах:
Т.е магний восстановил водород.