№2 ковалентная полярная связь
№3 ковалентная неполярная связь
№4
Хлорид калия -ионная решетка
Графит - атомная решетка
Водород - молекулярная решетка
Цинк - металлическая
№5 где?
№6
Cr2O3 - Cr(+3), O(-2)
Mg(OH)2 - Mg(+2), O(-2), Н(+1)
Н2СО3 - Н(+1), С(+5), О(-2)
FeSO4 - Fe(+2), S(+6), O(-2)
№7
A) Zn(0) + Fe(+2)S(+6)O4(-2) =Zn(+2)S(+6)O4(-2) + Fe(0) - это ОВР реакция
Б) Na(+)1l(-1)+ Ag(+1)N(+5)O3(-2) = Na(+1)N(+5)O3(-2) +Ag(+1)I(-1)
№8
Fe2O3 + 2Al = Al2O3 + 2Fe
Fe(+3) +3e = Fe(0)
Al(0) - 3e = Al(+3)
Fe2O3(Fe+3) - окислитель
Al(0) - восстановитель
№9. Степень окисления кальция равна +2
№10
При восстановлении степень окисления увеличивается
1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
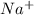

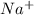
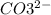

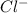
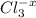


11г соли 99 г воды
Объяснение:
110 г -x
100- 10
11г