Объяснение:
1)
Дано:
m(K₂CO₃)=26,7г.
m(O)-?
1. Определим количество вещества карбоната калия, содержащего 1моль атомов кислорода:
1 моль K₂CO₃ содержит 3моль атомов кислорода
Х моль K₂CO₃ содержит 1моль атомов кислорода
Х моль K₂CO₃=0,33моль
2. Определим молярную массу карбоната калия:
M(K₂CO₃)=39x2+12+16x3=78+12+48=138 г./моль
3. Определим количество вещества карбоната калия в 27,6г.:
n(K₂CO₃)=27,6г/138 г./моль=0,2моль
4. Определим количество атомарного кислорода в 0,2моль карбоната калия:
0,33моль K₂CO₃) содержит 1моль атомов кислорода
0,2моль K₂CO₃) содержит Хмоль атомов кислорода
Х моль атомов кислорода=0,2мольх1моль/0,33моль=0,6моль
5. Масса атомарного кислорода в 0,6моль:
m(O)= 0,6мольx16г./моль=9,6г. кислорода
6. ответ: в 27,6г карбоната калия масса атомарного кислорода 9,6г.
2) M(NaCI)=23+35.5.=58,5г./моль
m(NaCI)=23г.+35,5г.= 58,5г.
m(Na)=23г.
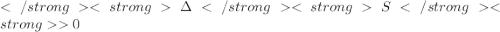
Объяснение:
В твердом состоянии вещество - более структурировано, нежели в газообразном; указанная реакция описывает превращение твердого графита в газообразный оксид углерода(II).
Энтропия - это мера неупорядоченности. Т.к. при разрушении/понижении степени структурированности возрастает число возможных взаиморасположений элементов, ("степеней свободы системы"), энтропия, отображающач это число, тоже растет, увеличивается. Величину изменения энтропии можно обозначить как ∆S.
В нашем случае значение энтропии возрастает, т.е.
∆S > 0
Поэтому ответ:
Энтропия возрастает; изменение энтропии происходит со знаком "+".
или
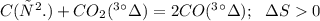
CaCl2+Na2CO3=CaCO3+2NaCl
Так как указано количество только соды, считаем что хлорид кальция находится в избытке или стехиометрическом соотношении и расчет количества продукта реакции рассчитываем по соде.
Атомный вес натрия Na=23
Атомный вес углерода С=12
Атомный вес кислорода О=16
Атомный вес кальция Ca=40
Молярный вес кальцинированной соды Na2CO3=23*2+12+16*3=106
Молярный вес карбоната кальция CaCO3=40+12+16*3=100
Мы взяли 200 граммов 5,3% раствора соды. Проценты - это количество вещества в 100 граммах смеси.
Таким образом мы взяли 200*5,3/100=10,6 граммов чистой 100% соды.
Теперь составляем пропорцию с учетом стехиометрических коэффициентов:
106 - 100
10,6 - Х
Х=10,6*100/106=10 граммов соды.
ответ: в результате данной реакции мы получим 10 граммов карбоната кальция.