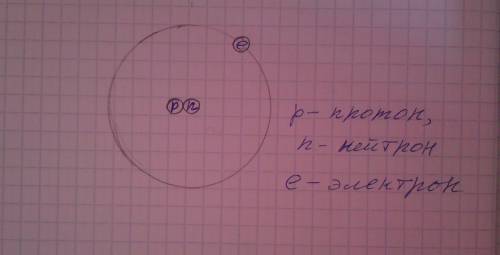
Дейтерий- стабильный изотоп водорода ( изотопы- разновидности атомов одного элемента различающиеся числом нейтронов и соответственно разными массовыми числами). Ядро атома дейтерия состоит из одного протона ( эл. частица с зарядом +) и одного нейтрона ( элементарная частица с зарядом 0) ,массовое число дейтерия равно двум. Количество нейтронов, можно вычислить, исходя из формулы A=Z+N, где А- массовое число, для дейтерия равное 2, - Z-число протонов, для дейтерия равное 1, тогда число нейтронов N=A-Z=2-1=1. Cхема строения( по Н. Бору) атома дейтерия -прилагаемый jpg- файл.
2) Необходимо уточнение условия задания, т.к. электроны являются носителями отрицательного заряда, то они не могут давать положительный заряд.
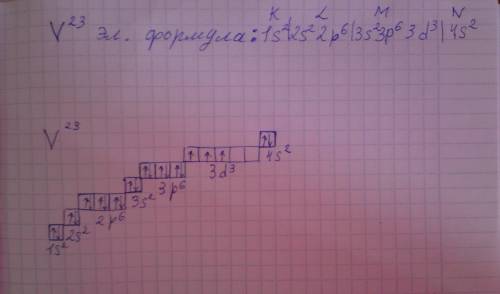
3) Атом с зарядом ядра +23 - это ванадий. V. Распределение электронов в атоме V по энергетическим уровням : К-уровень (1-ый)- 2 электрона; L( 2-ой)уровень - 8 электронов; М (3-ий)уровень- 11 электронов; N(4-ий)уровень- 2 электрона. Эл формула и электронно-графическая формула в прилагаемом jpg-файле.
Валентность +4, CO2 и SO2
Валентность +5, N2O5 и Br2O5
Объяснение:
NO валентность азота +2
SO3 валентность серы +6
CO2 валентность углерода +4
Br2O5 валентность брома +5
B2O3 валентность бора +3
SO2 валентность серы +4
N2O5 валентность азот +5