1.Из 18 г этанола было получено 12 г диэтилового эфира.Рассчитайте выход реакций дегидратаций. 2.Из образца нитробензола массой 13,00 г с выходом,равным 80%,получили анилин массой 7,44 г.Вычислите массовую долю примесей в исходном образце нитробензола.
Отнеситесь серьезно
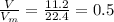 моль
моль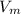 =0.25*22.4=5.6 л
=0.25*22.4=5.6 л
1.
Дано:
m(C₂H₅OH) = 18 гр
m пр(C₂H₅-O-C₂H₅) = 12 гр
Найти:
η(C₂H₅-O-C₂H₅) - ?
1) Для начала мы запишем уравнение реакций для получения диэтилового эфира из этанола, именно по такой уравнений реакций мы будем пользоваться:
2C₂H₅OH (H₂SO₄(конц.), t<140°C) → C₂H₅-O-C₂H₅ + H₂O
2) Для начала мы найдем количества вещества у этанола, а потом у диэтилового эфира по уравнению реакций:
M(C₂H₅OH) = 12×2 + 1×5 + 16 + 1 = 24 + 5 + 17 = 46гр/моль
n(C₂H₅OH) = m(C₂H₅OH)/M(C₂H₅OH) = 18 гр / 46 гр/моль ≈ 0,39 моль ⇒ n(C₂H₅-O-C₂H₅) = 1/2 × n(C₂H₅OH) = 1/2 × 0,39 моль = 0,195 моль - по уравнению реакций
3) Теперь находим теоретическую массу у диэтилового эфира:
M(C₂H₅-O-C₂H₅) = 12×2 + 1×5 + 16 + 12×2 + 1×5 = 24 + 5 + 16 + 24 + 5 = 74 гр/моль
m теор(C₂H₅-O-C₂H₅) = n(C₂H₅-O-C₂H₅) × M(C₂H₅-O-C₂H₅) = 0,195 моль × 74 гр/моль = 14,43 гр
4) Теперь находим выход реакций дегидратаций по такой формуле:
η(C₂H₅-O-C₂H₅) = m пр(C₂H₅-O-C₂H₅) / m теор(C₂H₅-O-C₂H₅) × 100% = 12 гр / 14,43 гр × 100% ≈ 0,832 × 100% ≈ 83,2%
ответ: η(C₂H₅-O-C₂H₅) = 83,2%
2.
Дано:
m(C₆H₅-NO₂) = 13,00 гр
η(C₆H₅-NO₂) = 80%
m пр(C₆H₅-NH₂) = 7,44 гр
Найти:
ω(примесей) - ?
1) Для начала мы запишем уравнение реакций для получения анилина из нитробензола, именно по такой уравнений реакций мы будем пользоваться:
C₆H₅-NO₂ + 3H₂ → C₆H₅-NH₂ + H₂O
2) Для начала мы найдем количества вещества у анилина полученной, а потом у нитробензола по уравнению реакций:
M(C₆H₅-NH₂) = 12×6 + 1×5 + 14 + 1×2 = 72 + 5 + 14 + 2 = 93 гр/моль
n пр(C₆H₅-NH₂) = m пр(C₆H₅-NH₂)/M(C₆H₅-NH₂) = 7,44 гр / 93 гр/моль = 0,08 моль ⇒ n пр(C₆H₅-NO₂) = n пр(C₆H₅-NH₂) = 0,08 моль
3) Теперь находим количества вещества у нитробензола в теоретической части:
η(C₆H₅-NO₂) = n пр(C₆H₅-NO₂) / n теор(C₆H₅-NO₂) × 100% ⇒ n теор(C₆H₅-NO₂) = (n пр(C₆H₅-NO₂)×100%)/η(C₆H₅-NO₂) = (0,08 моль × 100%)/80% = 0,08 моль × 1,25 = 0,1 моль
4) Теперь находим теоретическую массу у нитробензола:
M(C₆H₅-NO₂) = 12×6 + 1×5 + 14 + 16×2 = 72 + 5 + 14 + 32 = 123 гр/моль
m теор(C₆H₅-NO₂) = n теор(C₆H₅-NO₂) × M(C₆H₅-NO₂) = 0,1 моль × 123 гр/моль = 12,3 гр
5) Теперь находим массу примесей в исходном образце нитробензола:
m(примесей) = m(C₆H₅-NO₂) - m теор(C₆H₅-NO₂) = 13,00 гр - 12,3 гр = 0,7 гр
6) Теперь находим массовую долю примесей в исходном образце нитробензола:
ω(примесей) = m(примесей)/m(C₆H₅-NO₂) × 100% = 0,7 гр / 13,00 гр × 100% ≈ 0,054 × 100% ≈ 5,4%
ответ: ω(примесей) = 5,4%
Решено от :