Объяснение:
w(Эл.) = n * Ar(Эл.) / M(в-ва) ;
M(K₂MnO₄) = nAr(K) + nAr(Mn) + nAr(O) = 2* 39 + 55 + 4 * 16 = 197 г/моль
ω(K) = 2 * 39 / 197 = 0,396 = 39,6 %
ω(Mn) = 55 / 197 = 0,279 = 27,9 %
ω(O) = 4 * 16 / 197 = 0,325 = 32,5 %.
ответ: K=39,6% , Mn=27,9 % , O=32,5 %.
6) щелочи: NaOH, KOH, LiOH,Ca(OH)2
нерастворимые: Ti(OH)3, Mg(OH)2
9) KOH + HNO3= H2O + KNO3
n=m÷M
n(HNO3) = 18,9÷63= 0,3 моль
по уравнению следует, что: n(HNO3)= n(KNO3)=0,3 моль
m=n×M
m(KNO3) = 0,3 × 101= 30,3 г
ответ:30,3г
10) из дано этот элемент щелочноземельный металл, все ЩЗМ реагируют с азотом одинаково(азот восстанавливается до -3), примем щзм за Х:
3X+N2=X3N2
n= V÷Vm
(для газов при н.у. Vm=22,4 л/моль)
n(N2) = 1,12:22,4= 0,05 моль
по уравнению реакции: 3×n(N2)= n(X)
n(X)= 0,05×3= 0,15 моль
M=m÷n
M(X)=3,6÷0,15=24г/моль => Х - это Мg
схема электронного строения на фото
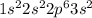
6) щелочи: NaOH, KOH, LiOH,Ca(OH)2
нерастворимые: Ti(OH)3, Mg(OH)2
9) KOH + HNO3= H2O + KNO3
n=m÷M
n(HNO3) = 18,9÷63= 0,3 моль
по уравнению следует, что: n(HNO3)= n(KNO3)=0,3 моль
m=n×M
m(KNO3) = 0,3 × 101= 30,3 г
ответ:30,3г
10) из дано этот элемент щелочноземельный металл, все ЩЗМ реагируют с азотом одинаково(азот восстанавливается до -3), примем щзм за Х:
3X+N2=X3N2
n= V÷Vm
(для газов при н.у. Vm=22,4 л/моль)
n(N2) = 1,12:22,4= 0,05 моль
по уравнению реакции: 3×n(N2)= n(X)
n(X)= 0,05×3= 0,15 моль
M=m÷n
M(X)=3,6÷0,15=24г/моль => Х - это Мg
схема электронного строения на фото
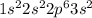
K — 39,6%; Mn — 27,9 %; O — 32,5 %.
Объяснение:
Mr(K₂MnO₄) = 39 · 2 + 55 + 16 · 4 = 197
ω(K) = 39 · 2 · 100 % / 197 = 39,6 %
ω(Mn) = 55 · 100 % / 197 = 27,9 %
ω(O) = 16 · 4 · 100 % / 197 = 32,5 %.