1) Положение в периодической таблице
Галлий - это элемент ІІІ группы, IV периода таблицы Менделеева. Он - металл. Порядковый номер – 31. Обозначение – Ga.
2)Особенности строения атома:
Положительно заряженное ядро (+31), внутри которого - 31 протон, а также 39 нейтронов, а вокруг же, движется 31 электрон, по четырем орбитам
Распределение электронов по орбиталям:
+31Ga)2)8)18)3
P.S: (Относится к элементам p-семейства).
3)Вид химической связи
Металлическая
4)Тип кристаллической решетки
Кристаллическая решетка галлия образована двухатомными молекулами, а не отдельными атомами, что очень необычно.
5) Физические свойства
Металл серебристо-белого цвета, мягкий, тяжёлый. Плотность - 5,9 г/см3. Удельная теплоемкость - 376,7 дж/(кг·К)
6) Химические свойства
Расплавленный галлий (t больше 300° С) взаимодействует со всеми металлами и сплавами (кроме W).
Галлий реагирует с водой: 2Ga + 4H2O = 2GaOOH + 3H2 (условия: тем-ра и давление)
2Ga + 6HCl = 2GaCl3 + 3H2 - реакция с кислотами. Протекает медленно
2Ga + 6H2O + 2NaOH = 2Na[Ga(OH)4] + 3H2 - растворяется в растворах щелочей (под тем-рой)
7) Получение
Из растворов Аl(ОН)3 галлий выделяют электролизом.
Из щелочного раствора, полученного после обработки водой, осаждают Ga(OH)3, который растворяют в щелочи, затем также выделяют галлий электролизом.
8) Применение
На основе галлия созданы практически металлические клеи.
Галлий используется при изготовлении оптических зеркал.
Применяются в солнечных батареях
А) 3)
Б) 1)
В) 1)
Г) 4)
Д) 2)
Объяснение:
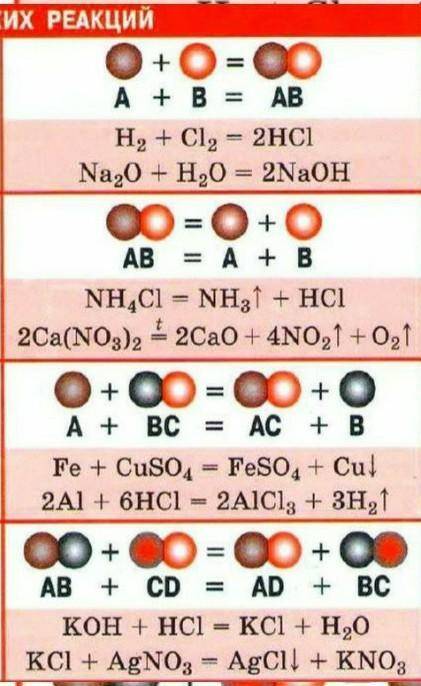
Типы реакции:
Реакция соединения - реакция образования одного сложного вещества при соединении двух или нескольких веществ.
Примеры:
Fe + S = FeS
СаО + Н2О = Са(ОН)2
Реакция разложения - разложение одного сложного вещества на несколько новых веществ. Примеры:
2HgO = 2Hg + O2
СаСО3 = СаО + СО2
Реакция замещения - реакция, протекающая между простыми и сложными веществами, при которой
атомы простого вещества замещают атомы одного из элементов в сложном
веществе.
Примеры:
Fe + CuSO4 = FeSO4 + Cu
Zn + 2HCl = ZnCl2 + H2
Реакция обмена - реакция, протекающая между двумя сложными веществами с образованием двух других сложных веществ.
Пример:
MgO + H2SO4 = MgSO4 + Н2О

Кислоты - химические соединения отдавать катион водорода, либо соединения принимать электронную пару с образованием ковалентной связи.
Основание - это сложные вещества, при диссоциации которых в водных растворах отщепляется только один вид анионов - гидроксид-ионы OH−.
Соли с позиции теории элект. диссоциации - это вещества, при растворении в воде дающие положительно заряженные ионы металла (или аммония NH4+) и отрицательно заряженные ионы кислотных остатков.