1. соль двухвалентного железа и соляной кислоты. если у атома железа валентность 2, то у 2х атомов хлора по 1 на каждый
2. соляная кислота. у водорода постоянная валентность 1, у хлора значит тоже 1
3. хлористый алюминий. тут хлор имеет валентность 1, значит железо 3х валентное
4. оксиген всегда 2х валентный, значит у азота валентность 2*2=4
5. оксиген всегда 2х валентный,значит у меди валентность 2
6. кальций всегда 2х валентный,значит у хлора валентность 1 на каждый атом
7. оксиген всегда 2х валентный,значит у свинца тоже валентность 2
8. оксиген всегда 2х валентный,значит у хрома валентность 6/2=3
9. водород всегда 1-валентный, значит у серы валентность 2
10. оксиген всегда 2х валентный,значит у хрома валентность 2*3=6
В большинстве случаев валентность и степень окисления численно совпадают
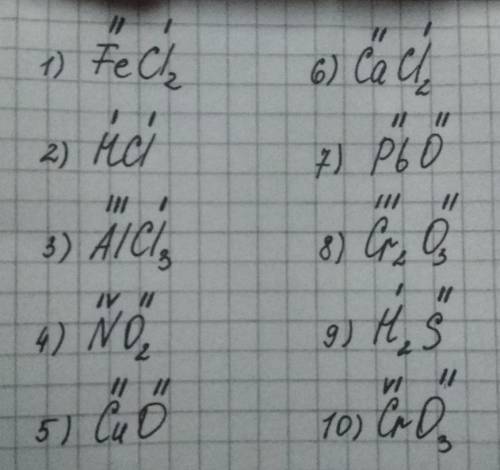
A)Mg{+2}(NO3)2{-}+2K{+}OH{-}=Mg{+2}(OH)2{-}(осадок)+2K{+}NO3{-}
Mg+(NO3)2+2K+2OH=Mg(OH)2(осадок)+2K+2NO3
Mg+OH=Mg(OH)2(осадок)
Б)К2{+}СО3{-2}+Ca{+2}(NO3)2{-}=2K{+}NO3{-}+Ca{+2}CO3{-2}(осадок)
K2+CO3+Ca+(NO3)2=2K+2NO3+CaCO3(осадок)
Ca+CO3=CaCO3(осадок)
B)2H{+}NO3{-}+Zn{+2}Cl2{-}=Zn{+2}(NO3)2{-}+2H{+}Cl{-}
2H+2NO3+Zn+2Cl=Zn+2NO3+2H+2Cl
Обратимая реакция!
С)Hg{+2}Cl2{-}+Cu{+2}(NO3)2{-}=Hg{+2}(NO3)2{-}+Cu{+2}Cl2{-}
Hg+2Cl+Cu+2NO3=Hg+2NO3+Cu+Cl2
Обратимая реакция!
В такие скобки { и } писал степень окисления.
Окислительно-восстановительная реакция:
2Са + О₂ = 2СаО
Реакция разложения ( не окислительно-восстановительная):
СаСО₃ = СаО + СО₂