Объяснение:
Все задачи 2-5 однотипные и решаются по одной идее.
Пусть M - это молекулярная масса вещества, A(Э) - атомная масса условного химического элемента Э, n - количество атомов в строении молекулы.
Тогда массовая доля элемента в молекуле будет составлять:
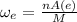
Тогда, зная массовую долю вещества, можно найти количество атомов по формуле:
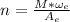
Идея решения таких задач сводится к составлению соотношений индексов атомов: ведь
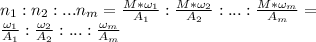
То есть достаточно взять соответствующие отношения массовых долей элемента к атомной массе и составить соотношения между отношениями.
Если решать задачу 2, атомная масса магния = 24, кислорода = 16. Тогда имеет место:
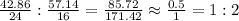
Простейшая формула, соответствующая отношению, выглядит как MgO₂.
Теперь, если дана молекулярная масса, нетрудно отыскать и истинную формулу. Пусть n - единица соотношения (1 : 2). Тогда 24n - масса магния, которая должна быть в соединении, 32n - масса кислорода. Справедливо уравнение:
24n + 32n = 56
56n = 56
n = 1
Значит истинная формула соединения - это MgO₂
Остальные задачи решаются так же, только другие числа будут.
Определяем молекулярную массу вещества, складывая атомные массы ( из Периодической системы элементов Д.И.Менделеева), умноженные на индексы, представленные в формуле вещества:
Mr(Na₂CO₃) = 2·23 +12 + 3·16 = 106г/моль.
Концентрация Cm требуемого раствора 0,2М, т.е. 0,2моль в 1 л раствора. А его надо V =2 л:
m = Cm·Mr·V = 0,2моль/л·106г/моль·2л = 42,4г
Формулу для определения массы вещества, необходимого для получения требуемого объема заданной концентрации, хорошо бы запомнить: обязательно пригодится и в школе, и в домашнем хозяйстве!