Рассчитать, какая масса кислорода потребуется для реакции с 44,8 г железа Схема реакции: Fe + O2 → Fe2O3 m(Fe) = 44,8 г m(O2) - ? можно с объяснением !
1. реакции соединения при реакциях соединения из нескольких реагирующих веществ относительно простого состава получается одно вещество более сложного состава: a + b + c = d как правило, эти реакции выделением тепла, т. е. приводят к образованию более устойчивых и менее богатых энергией соединений. реакции соединения простых веществ всегда носят окислительно-восстановительный характер. реакции соединения, протекающие между сложными веществами, могут происходить как без изменения валентности: сасо3 + со2 + н2о = са (нсо3)2, так и относиться к числу окислительно-восстановительных: 2fесl2 + сl2 = 2fесl3. 2. реакции разложения реакции разложения приводят к образованию нескольких соединений из одного сложного вещества: а = в + с + d. продуктами разложения сложного вещества могут быть как простые, так и сложные вещества. из реакций разложения, протекающих без изменения валентных состояний, следует отметить разложение кристаллогидратов, оснований, кислот и солей кислородсодержащих кислот: to cuso4 5h2o=cuso4 + 5h2o to cu(oh)2=cuo + h2o to h2sio3=sio2 + h2o. к реакциям разложения окислительно-восстановительного характера относится разложение оксидов, кислот и солей, образованных элементами в высших степенях окисления: to 2so3=2so2 + o2. to 4hno3=2h2o + 4no2o + o2o. 2agno3 = 2ag + 2no2 + o2, (nh4)2cr2o7 = cr2o3 + n2 + 4h2o. особенно характерны окислительно-восстановительные реакции разложения для солей азотной кислоты. реакции разложения в органической носят название крекинга: с18h38 = с9h18 + с9h20, или дегидрирования c4h10 = c4h6 + 2h2. 3. реакции замещения при реакциях замещения обычно простое вещество взаимодействует со сложным, образуя другое простое вещество и другое сложное: а + вс = ав + с. эти реакции в подавляющем большинстве принадлежат к окислительно-восстановительным: 2аl + fe2o3 = 2fе + аl2о3, zn + 2нсl = znсl2 + н2, 2квr + сl2 = 2ксl + вr2, 2ксlo3 + l2 = 2klo3 + сl2. примеры реакций замещения, не изменением валентных состояний атомов, крайне немногочисленны. следует отметить реакцию двуокиси кремния с солями кислородсодержащих кислот, которым отвечают газообразные или летучие ангидриды: сасо3+ sio2 = саsio3 + со2, са3(ро4)2 + зsio2 = зсаsio3 + р2о5, иногда эти реакции рассматривают как реакции обмена: сн4 + сl2 = сн3сl + нсl. 4. реакции обмена реакциями обмена называют реакции между двумя соединениями, которые обмениваются между собой своими составными частями: ав + сd = аd + св. если при реакциях замещения протекают окислительно-восстановительные процессы, то реакции обмена всегда происходят без изменения валентного состояния атомов. это наиболее распространенная группа реакций между сложными веществами - , основаниями, кислотами и солями: zno + н2sо4 = znsо4 + н2о, agnо3 + квr = аgвr + кnо3, сrсl3 + зnаон = сr(он) 3 + зnасl. частный случай этих реакций обмена - реакции нейтрализации: нсl + кон = ксl + н2о. обычно эти реакции подчиняются законам равновесия и протекают в том направлении, где хотя бы одно из веществ удаляется из сферы реакции в виде газообразного, летучего вещества, осадка или малодиссоциирующего (для растворов) соединения: nансо3 + нсl = nасl + н2о + со2↑, са (нсо3)2 + са (он) 2 = 2сасо3↓ + 2н2о, сн3сооnа + н3ро4 = сн3соон + nан2ро4.
Попытаюсь Данные, которыми мы располагаем: Нам дан 10%-ый раствор йода. В сумме должно выйти 100г раствора. Плотность спирта равна 0,8г/см3. Попробуем применить их: Для решения задачи мы должны знать формулу P = [М(вещ-ва) : М(Раствора)]*100%. (На бумаге она красивее: тут не слишком удобно писать такие формулы) Р у нас равно 10% М(р-ра) у нас равна 100г Нам необходимо найти М(вещ-ва), а в данном случае это йод. 1) 10%=[x:100г]*100% => x=[10%*100г]:100%=0,1*100г=10г (Масса йода) 2) 100г-10г=90г (Мы отнимаем 10г, т.к. раствор это вещество + растворитель. В данном случае у нас йод + спирт и, чтобы узнать сколько грамм спирта в растворе, нам надо отнять от раствора массу вещ-ва) 3) p=m:V => V=m:p => V(спирта)=90г:0,8г/см3=112,5см3 (Объём спирта) ответ: Потребуется 112,5см3 спирта.
Если что-то осталось непонятным - спрашивай! :)
получения кристаллического йода из йодной настойки в домашних условиях это смешать йод с холодной водой, положить уже полученный раствор в холодильник (примерно на час), а потом просто слить жидкость. В результате на дне получим йод.
Дано :
m(Fe) = 44,8 г.
Найти :
m(O₂) = ?
Уравнение химической реакции —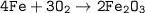 .
.
По уравнению реакции — n(Fe) : n(O₂) = 4 : 3, отсюда следует, что 3n(Fe) = 4n(O₂) ⇒ n(O₂) =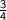 *n(Fe).
*n(Fe).
Найдём количество вещества железа —
n(Fe) = m(Fe) : M(Fe) = 44,8 г : 56 г/моль = 0,8 моль.
Тогда по выше сказанному — n(O₂) =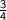 *n(Fe) =
*n(Fe) = 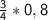 моль = 0,6 моль.
моль = 0,6 моль.
Найдём массу кислорода —
m(O₂) = n(O₂)*M(O₂) = 0,6 моль*32 г/моль = 19,2 г.
19,2 г.