
Дано:
m(Zn) = 20г.
Wприм.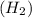 = 0,1 = 10%
= 0,1 = 10%
Найти:
Vчист.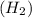 - ?
- ?

1. При условии, что Wприм., именно водорода, равна 10%!
1) n(Zn) = m(Zn) / M(Zn) = 20г. / 65 г/моль = 0,3 моль;
2) По уравнению реакции n(Zn) = n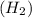 = 0,3 моль;
= 0,3 моль;
3) V с прим.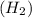 = n
= n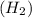 * Vm = 6,89 л.;
* Vm = 6,89 л.;
4) W чист. в-ва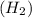 = 100% - Wприм.
= 100% - Wприм.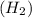 = 100% - 10% = 90%;
= 100% - 10% = 90%;
5) Рассчитаем объём чистого водорода, составив пропорцию, где x (л.) - объём чистого водорода:
6,89 л. - 100%
x л. 90% => x л. = 6,89 л. * 90% / 100% = 6,2 л.
ответ: Vчист.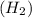 = 6,2 л.
= 6,2 л.
2. Если ты имела в виду, что примеси соляной кислоты, то тогда 4) и 5) действие делать не надо! Объём водорода будет равен 6,89 л.!
Я думаю, скорее всего там давали примеси водорода, поскольку здесь вести рассчёты с соляной кислотой нет смысла!
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
задача №6 Na2CO3 + 2HCl = CO2 + 2NaCl + H2O
m(HCl) = m(p-paHCl)*W(HCl) = 150*0,3 = 45 г.
n(HCl) = m(HCl)/M(HCl) = 45/36,5 = 1,23 моль
По уравнению видно, что соотношение Na2CO3 и HCl равняется 1:2. Соотношение имеющихся моль карбоната натрия и соляной кислоты 0,5:1,23 или 1:2,46. Отсюда видно, что кислота в избытке, значит карбонат прореагировал полностью, потому по нему и считаем.
Из уравнения же видно, что СО2 выделяется столько же (в моль) сколько имеется карбоната натрия: n(CO2) = n(Na2CO3) = 0,5 моль.
V(CO2) = Vm*n(CO2) (Vm - молярный объем, равен 22,4 л/моль при н.у.)
V(CO2) = 22,4*0,5 = 11,2 л.
Задача №7
Извини,но я не знаю как ее решать