25,6 г 24,6 г,х г у г
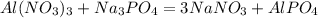
213 г 141 г 122 г
1. Определим,какое из исходных веществ прореагирует полностью(без остатка),приняв,например,массу фосфата натрия:
для полного взаимодействия 213 г нитрата алюминия необходимо 141 г фосфата натрия, а -- // -- 25,6 г____________________________х г, откуда
х=25,6*141/213=16,95 г
2. Как видим,что фосфат натрия дан в избытке,то расчет массы осадка ведем по массе нитрата алюминия:
при взаимодействии 213 г нитрата образуется 122 г фосфата алюминия,а
при -- // -- 25,6 г_________________у г, откуда
у=25,6*122/213=14,7 г
3. Чтобы найти количество вещества,необходимо сначала найти массу излишка,отняв от общей массы фосфата натрия массу,которая пошла на реакцию,т.е. 24,6-16,95=7,65 г
4. А теперь отнеся эту массу к молярной массе фосфата натрия,и получим количество вещества:
v(излишка)=m(излишка)/M(Na3PO4)=7,65/141=0,05 моль
х г 34,95 г
1. 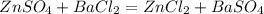
161 г 233 г
Найдем массу сульфата цинка:
при взаимодействии 161 г сульфата цинка выпадает 233 г сульфата бария,а
при -- // -- х г_______________________34,95 г, откуда
х=161*34,95/233=24,15 г
у г 39,4 г
2. 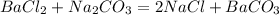
106 г 197 г
Найдем массу карбоната натрия:
при взаимодействии 106 г карбоната натрия выпадает 197 г карбоната цинка,а
при -- // -- у г___________________________39,4 г, откуда
у=106*39,4/197=21,2 г
24,15 г 21,2 г,k г z г
3. 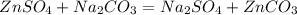
161 г 106 г 125 г
1) определим,какое из исходных веществ прореагирует полностью(без остатка),приняв массу карбоната натрия за k:
для полного взаимодействия 161 г сульфата необходимо 106 г карбоната, а
для -- // -- 24,15 г__________________k г, откда
k=24,15*106/161=15,9 г
2) как видим,что карбоната натрия дано в избытке,значит массу осадка рассчитываем по массе сульфата цинка:
при взаимодействии 161 г сульфата цинка выпадает 125 г карбоната цинка, а
при -- // -- 24,15 г______________________z г, откуда
z=24,15*125/161=18,75 г
1-3. ch3-ch3 = ch2=ch2 + h2 - дегидрирование алканов до алкенов
2-? ch3-ch3 + cl2 = ch3-ch2cl + hcl (ничего не подходит)
3-2. ch4 + cl2 = ch3cl + hcl