22,4
Объяснение:
Дано:
m(CaO) = 112 г
Найти:
V(O₂) = ?
Реакция: 2Ca + O₂ → 2CaO
Сначала находим количество вещества оксида кальция:
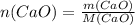 , где M(CaO) - молярная масса CaO, которая считается как сумма атомных масс Ca и O (даны в таблице Менделеева)
, где M(CaO) - молярная масса CaO, которая считается как сумма атомных масс Ca и O (даны в таблице Менделеева)
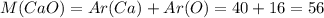 г/моль
г/моль
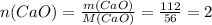 моль
моль
По реакции видно, что оксида кальция в 2 раза больше, чем затраченного кислорода (по коэффициентам смотрим: у CaO 2, у O₂ 1). Поэтому и количество вещества у кислорода будет в 2 раза меньше, чем у оксида кальция:
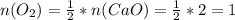 моль
моль
Объем считаем по формуле:
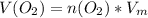 , где
, где 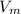 - молярный объем, который для всех газов при н.у. равен 22,4 л/моль.
- молярный объем, который для всех газов при н.у. равен 22,4 л/моль.
Подставляем и решаем:
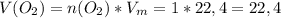 л
л
ответ: 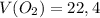 л
л
ответ:это все что я могу сделать извини
2.Некорректное условие.
Угольная кислота это раствор, значит с объемом кислоты должна быть массовая доля и плотность.
Если речь идет про массу угольной кислоты и масса ее 140 г
то вот вам решение
H2CO3 = CO2+H2O
1. Находим n(угольной кислоты)
M(H2CO3 )= 62г/моль
n(H2CO3) = m(H2CO3)/M(H2CO3 ) = 140 /62= 2,26моль
по уравнению на 1 моль H2CO3 приходится CO2
значит, если взять2,26мольH2CO3 то n(CO2) = 2,26моль
2. V(CO2) = n(CO2)* Vm
Vm = 22.4 дм4/моль.
V(CO2) = 2,26моль*22.4 дм4/моль = 50,6дм3
Объяснение: