Объяснение:
1) 1)C3H8 (t) = C3H6 +H2 - реакция дегидрации (разложения)
2)H2C=CH-CH3 + H2O (кат) - H3C-CH(OH)-CH3
3) H3C-CH(OH)-CH3 + O2 (t) - H3C-C(O)-CH3 + H2O
4) 2H3C-C(O)-CH3 +3O2 (t) = 2CH3COOH + 2HCOOH
5) CH3COOH + Cl2 = ClCH2-COOH + HCl
ClCH2-COOH + NH3 = NH2-CH2-COOH + HCl
4NH2-CH2-COOH + 9O2 = 2N2 + 8CO2 + 10H2O
2) Тушение горящего водой проводить нельзя: магний крайне активный металл, который взаимодействует с водой со взрывом и усилением горения:
Mg + 2H2O = Mg(OH)2 + H2
3) R-13B1 - CF3Br ; R-116 - C2F6 ; по правилам номенклатура фреонов, самая правая цифра - количество атомов фтора, следующая за ней - количество атомов водорода + 1, самая левая - количество атомов углерода - 1; если в составе фреона есть атомы Br они показываются буквой B стоящей в конце названия, после буквы стоит цифра ю, указывающая количество атомов Br, перед бромом номенклатура по цифрам сохраняется
4) {m[AgI] * nI(-) * (n-x)Na(+)} ^x(-) *xK(+)
5) V (Hg) = m(Hg) /p(Hg) = 5.2 * 13,59 = 0.383 (см3)
S = Sуд * V ; V= Sуд/S ; Sуд =4пr2/4/3пr3
V = 3/92.2r
V(частица) / V(Hg) = 0.085r
V(частицы) = 4/3пr^3 = 0.085r
4.19r^3 = 0.085r |r
4.19r^2 = 0.085
2.05r = 0.29
r = 0.14 (м)
D=2r = 0.28 (м)
прощение за кривоватость написания на картинках, в дороге + в заметках не так удобно писать, нежели на бумаге. Также предупреждаю, что ОЧЕНЬ МНОГО БУКВ, поскольку старалась объяснить всё как можно подробнее и понятнее.
Объяснение: любые вещества состоят из молекул, а те, в свою очередь, из атомов. Для наглядности, представьте, что атомы - шарики, вокруг которых, как планеты вокруг Солнца в нашей системе, крутятся более маленькие шарики - электроны, - заряженные отрицательно.
Для того, чтобы между разными веществами проходили разные реакции, электроны отсоединяются от одного атома и присоединяются к другому, тем самым связывая их (не буду описывать все процессы, это уже физика, нежели химия).
Сейчас буду говорить не научным языком, просто для того, чтобы было понятно.
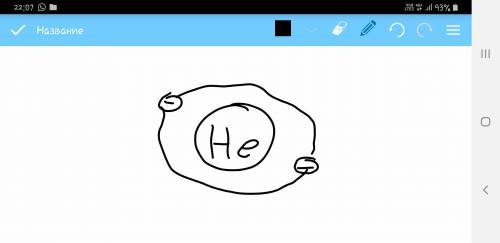
Как и в Солнечной системе, электроны расположены ближе или дальше от атома. Все электроны заряжены отрицательно, поэтому, если вспомнить физику, можно понять: раз они все имеют одинаковый заряд (отрицательный в нашем случае), значит, они должны друг от друга отталкиваться. Чтобы этого не произошло, между электронами должны быть расстояния. Именно поэтому часть электронов могут быть расположены на одном расстоянии от атома с разным расстоянием друг от друга, а другие переходят на более дальние от атома уровни (рисунок 3, пример на гелие). Всем лень рисовать каждый раз эти все кружочки, да и в принципе из-за разных нюансов это сделать сложно, поэтому придумали записывать всё ввиде схем (рисунок 2): стрелочки - сам электроны. Вообще, расположение электронов относительно атома несколько сложнее. Мало того, что они на разных расстояниях (электронных уровнях) от атома, так ещё и электроны, которые находятся на одном таком уровне, могут быть на разных подуровнях (рисунок 4), т.е. вроде на одном расстоянии от атома, но всё же один ближе, а другой - дальше. Для того, чтобы не путаться в подуровнях, их назвали буквами s, p, d, f. Соответственно электроны, находящиеся на этих подуровнях, называют s-, p-, d- и f-электронами. Они отличаются друг от друга формой (s-электроны - круглые, p-электроны - как знак бесконечности, только объёмный, и т.п.).
Электронные уровни обозначаются цифрами. 1 - самый близкий к атому, потом 2, 3 и т.д.
Теперь к самому заданию. От нас требуется расписать, сколько уровней у атома, электронов на этих уровнях и т.п.
Всегда:
У первого уровня - максимум 2 электрона
У второго - 8
У третьего - 16
У четвёртого - 32
У пятого - 32
У шестого - 16
....
У каждого подуровня также есть своё максимальное число электронов: s - 2 электрона, p - 6, d - 10, f - 14.
Итак, в задании у нас элемент под номером 16. В таблице Менделеева - сера (S). Рисунок 1.
+16 - число протонов - положительно заряженые частицы внутри атома, их число равно числу электронов (чтобы в сумме они по заряду давали 0), поэтому электронов у нас тоже 16. Группа в таблице Менделеева (столбик) определяет число электронов на последнем уровне, т.е. у серы их 6, а период (горизонталь) - число электронных уровней, т.е. у серы их 3.
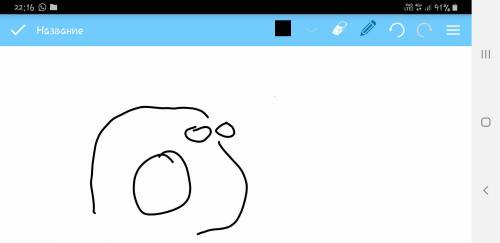
Уровни записываем дугами, поэтому их на рисунке 3. Под ними цифры (2, 8, 6) - число электронов на каждом уровне. Самый дальний уровень - самый последний, на нём 6 электронов, поэтому там число 6. Самый ближний уровень - первый, на нём 2 электрона, поэтому цифра 2. Между ними уровень - предпоследний. Для того, чтобы определить, сколько электронов на предпоследнем уровне, нужно сложить число электронов, которые мы уже проставили (2+6=8) и вычесть их из общего числа электронов (16-8=8). Ставим у этого уровня 8.
Теперь начинаем расписывать подуровни.
У первого уровня 2 электрона, у s-подуровня максимум тоже 2, поэтому пишем 1s² (1 - номер уровня, ² - число электронов, записывается как степень). Дальше идёт 2 уровень, там 8 электронов: 2s², остаётся 8-2=6 электронов. Начинается p-подуровень, где максимальное число электронов - 6, поэтому у второго уровня электронная конфигурация такая: 2s²2p⁶.
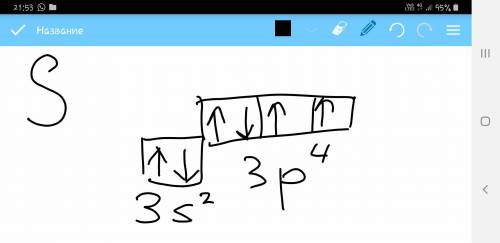
С третьим уровнем аналогично: 3s², остаётся 6-2=4 электрона. p-подуровень их спокойно умещает, просто будет не до конца заполнен, получается 3s²3p⁴.
Итого: 1s²2s²2p⁶3s²3p⁴.
На рисунке 2 я привела пример, как на схеме записывается расположение электронов у серы на последнем уровне (3). У p-подуровня сначала заполняются слева направо все клеточки по одному электрону, а потом слева направо начинают вписывать другие электроны (если есть). В каждой клетке может быть или 1, или 2 электрона, не больше. Это сделали для удобства, чтобы показать, что электроны как бы парочками ходят.
Всё. Если что-то непонятно - спрашивайте. И ещё раз извините, что кривые рисунки и много букв)

2) вычтем из оксида примеси, чтобы вычислить массу чистого железа: 64-9,6=54,4
3) найдем массовую долю железа : 54,4/64=0,85*100=85%
как-то так)