Задача №1
Формула нахождения объема:
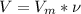 , здесь
, здесь 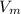 - молярный объем, равный 22,4 л/моль,
- молярный объем, равный 22,4 л/моль,  - количество вещества
- количество вещества
Подставляем:
V = 2моль*22,4л/моль = 44,8 литров
Эадача №2
Для этого воспольхуемся следующими формулами:
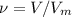
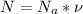 ,
, 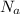 - число Авогадро =
- число Авогадро = 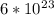 молекул
молекул
Воспользуемся первой формулой, и найдем количество вещества:
 = 44.8л/22,4л/моль = 2 моль
= 44.8л/22,4л/моль = 2 моль
теперь воспользуемся второй формулой:
N = 2 * 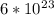 молекул =
молекул = 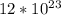 молекул
молекул
Задача №3
Для решения этой задачки воспользуемся следующими формулами:
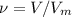
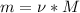
Воспользуемся первой формулой и найдем количество вещества:
 = 11.2л/22,4л/моль = 0,5 моль
= 11.2л/22,4л/моль = 0,5 моль
Воспользуемся второй формулой и найдем массу:
m = 0,5моль * 2л/моль = 1 грамм
Задание №4
Кислоты:
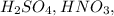
Соли:
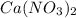 ,
, 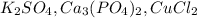
Оксиды: 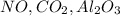
Напишемо рівняння реакції ефірифікації для бутилового спирту (C4H9OH) і пропилового спирту (C3H7OH):C4H9OH + C3H7OH → C4H9OC3H7 + H2OЗа вихідні речовини взято маси, які дорівнюють 20 г для бутилового спирту і 30 г для пропилового спирту. Щоб знайти об'єм ефіру, який утвориться, потрібно обчислити мольну кількість кожного спирту за до моллярної маси і використати стехіометричні коефіцієнти з рівняння реакції, щоб знайти мольну кількість утвореного ефіру. Після цього можна обчислити масу ефіру за до мольної маси.1) Найдемо мольну кількість бутилового спирту:n(C4H9OH) = m(C4H9OH) / M(C4H9OH) = 20 г / 74,12 г/моль = 0,27 моль2) Найдемо мольну кількість пропилового спирту:n(C3H7OH) = m(C3H7OH) / M(C3H7OH) = 30 г / 60,10 г/моль = 0,50 моль3) Оскільки реакція є стехіометричною, мольний співвідношення між бутиловим спиртом і пропиловим спиртом 1:1. Тому реагує 0,27 моль бутилового спирту і 0,27 моль пропилового спирту, що призведе до утворення 0,27 моль ефіру.4) Знайдемо масу утвореного ефіру:m(C4H9OC3H7) = n(C4H9OC3H7) * M(C4H9OC3H7) = 0,27 моль * 130,23 г/моль = 35,12 г
Отже, об'єм утвореного ефіру неможливо визначити без додаткової інформації про його щільність або об'ємну частку.