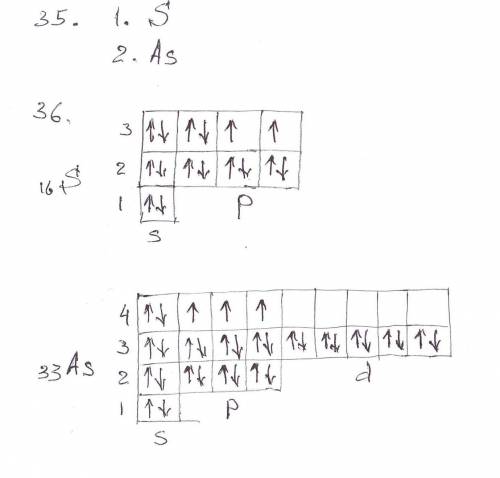
36. Дописать название подуровня и его номер. Записать химический знак элемента и перед ним поставить его порядковый номер. (См. в файл)
37. Номеру данного периода.
38. Номеру группы.
39. Количеством валентных электронов, т.е. электронов на внешнем слое.
40. Изменением строения их электронных оболочек. В каждом периоде происходит заполнение электронами внешнего энергетического уровня до восьми. Следовательно, электронные конфигурации наружных энергетических уровней периодически повторяются.
41. s-элементы - это элементы главной подгруппы I и II групп. По факту это элементы у которых заполняется s-уровень. В каждом периоде по 2 s-элемента.
42. р-элементы - это элементы III-VIII групп, главных подгрупп. Это элементы у которых заполняется р-уровень. Всего 6 р-элементов в каждом периоде (кроме первого, их там нет; и седьмого - хотя там тоже их 6 штук).
43. d-элементы - это элементы I-VIII групп, побочных подгрупп. Это элементы у которых заполняется d-уровень. В каждом большом периоде по 10 d-элементов.
Объяснение:
Дано:
m(технического CaCO₃)=800г.
ω%(примесей в CaCO₃ )=12,%
Vm=22,4л./моль
V(CO₂)-?
1. Определим массу чистого карбоната кальция:
m(CaCO₃)=m(технического CaCO₃)xω%(примесей в CaCO₃ )÷100%
m(CaCO₃)=800г.×12,%÷100%=96г.
2. Определим молярную массу карбоната кальция и его количество вещества в 96г:
M(CaCO₃)=100г./моль
n₁(CaCO₃)=96г÷100г./моль=0,96моль
3. Запишем уравнение реакции разложения карбоната кальция:
CaCO₃ = CaO + CO₂
по уравнению реакции:
n(CaCO₃)=n(CO₂)=1моль
по условию задачи:
n₁(CaCO₃)=n₁(CO₂)=0,96моль
4. Определим объем оксида углерода(IV) :
n₁(CO₂)=0,96моль
V(CO₂)=n₁(CO₂)x22,4л./моль
V(CO₂)=0,96мольх22,4л./моль=21,5л.
5. ответ: при разложении 800г. технического карбоната кальция с массовой долей примесей 12% образовалось 21,5л. углекислого газа (оксида углерода(IV).
Звичайний чай містить воду (H₂O), цукор (C₁₂H₂₂O₁₁) та лимонну кислоту (C₆H₈O₇).
Для обчислення відносних молекулярних мас речовин потрібно врахувати атомні маси всіх елементів, що входять у склад молекул. Отже:
Вода (H₂O):
Водень (Н): 1.01 г/моль * 2 = 2.02 г/моль
Кисень (О): 16.00 г/моль * 1 = 16.00 г/моль
Відносна молекулярна маса води (H₂O) = 2.02 г/моль + 16.00 г/моль = 18.02 г/моль
Цукор (C₁₂H₂₂O₁₁):
Вуглець (С): 12.01 г/моль * 12 = 144.12 г/моль
Водень (Н): 1.01 г/моль * 22 = 22.22 г/моль
Кисень (О): 16.00 г/моль * 11 = 176.00 г/моль
Відносна молекулярна маса цукру (C₁₂H₂₂O₁₁) = 144.12 г/моль + 22.22 г/моль + 176.00 г/моль = 342.34 г/моль
Лимонна кислота (C₆H₈O₇):
Вуглець (С): 12.01 г/моль * 6 = 72.06 г/моль
Водень (Н): 1.01 г/моль * 8 = 8.08 г/моль
Кисень (О): 16.00 г/моль * 7 = 112.00 г/моль
Відносна молекулярна маса лимонної кислоти (C₆H₈O₇) = 72.06 г/моль + 8.08 г/моль + 112.00 г/моль = 192.14 г/моль
Таким чином, відносні молекулярні маси речовин складають:
Вода (H₂O): 18.02 г/моль
Цукор (C₁₂H₂₂O₁₁): 342.34 г/моль
Лимонна кислота (C₆H₈O₇): 192.14 г/моль