Объяснение:
Для определения валентности одного из элементов в бинарном соединении, делаем следующее
1) Указываем валентность у элемента, у которого она неизменна (например у кислорода II, у водорода I. Элементы с постоянной валентностью есть в учебнике, кроме того можно периодической системы: у элементов 1 главной группы всегда 1, у 2 - всегда 2)
II
Mn2O7
2) Умножаем валентность известного элемента на его индекс. Для данной молекулы валентность 2, индекс 7 , 2*7=14
3) Полученное число (14) делим на индекс второго элемента.
Индекс при марганце равен 2
14/2=7 - валентность марганца
4) В сложных соединениях с тремя и более элементами свои заморочки - сумма валентностей кислорода равна сумме валентностей остальных элементов
Например, серная кислота Н2SO4
валентность кислорода =2, их 4 штуки 4*2=8 валентных единиц
у водорода валентность =1, их 2, 2*1=2 валентных единицы.
Сера тут одна, сумма валентностей серы и водорода равна сумме валентностей кислорода, чтобы найти серу нужно от 8(кислород) отнять 2(водород)=6 - валентность серы
Валентность— это мера атомов к образованию ковалентных связей. Другими словами, сколько связей может образовать данный атом — такая у него и валентность; сколько он образовал — такая и степень окисления.
Чтобы определить валентность, сначала распиши формулу данного тебе вещества, а после — последние электронные слои атома элемента в этом веществе, валентность которого тебе нужно определить, и атомов элементов, близ лежащих с ним.
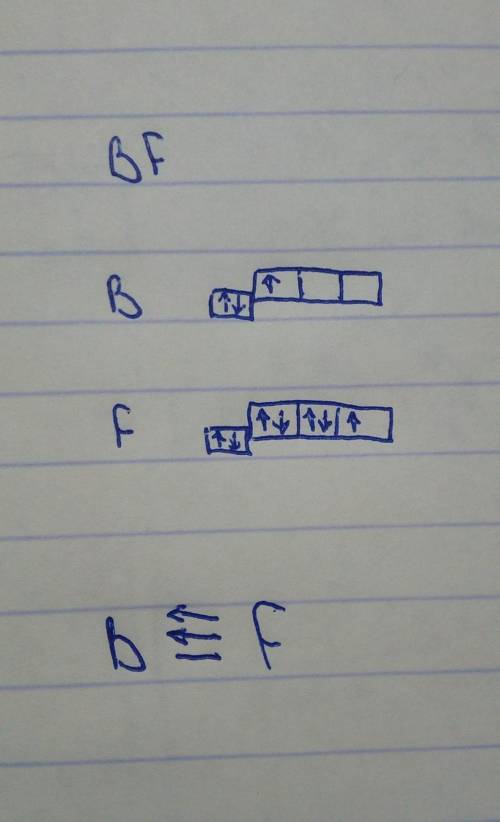
Например, возьмём BF (фторид бора). Между B и F будет тройная связь: все три — ковалентные (мы рассчитываем только по ковалентным!!), одна образована по обменному механизму(каждый из атомов отдал по одному электрону для образования пары электронов), а две по донорно-акцепторному(один атом отдал пару электронов, а другой предоставил место для этой пары). Как мы это узнали? Просто расписав их электронные конфигурации и рассмотрев последний слой, мы и увидим, что у бора есть 1 неспаренный электрон и 2 вакантные орбитали, а у фтора — 1 неспаренный электрон и непаделенные пары, которые как раз и перейдут к бору на те 2 свободные орбитали.
Таким образом в образование связи BF участвовало три пары электронов, поэтому валентность = 3 (как у бора, так и у фтора), но связь между ними только одна (просто она тройная), поэтому степень окисления бора +1, а фтора -1.
Вообще, есть ряд элементов, у которых валентность может быть только одна, ну и тот же кислород, который, как мы должны запомнить, в органике всегда четврехвалентен...
C) 0,2г. D) 2г. E) 500г.
6.Массовая доля углерода в карбонате кальция CaCO3
B) 12%
7.Верное утверждение физического свойства кислорода
E) Кислород тяжелее воздуха.
8.К амфотерному оксиду относится
. C) Оксид германия.
9.Утверждение, относящееся к химическому элементу водороду
E) Водород входит в состав воды.
10.Одноосновная кислота
E) Соляная
11.Кислая соль
A) KHSO4
12.Вода при комнатной температуре взаимодействует с
E) Калием.
13.У алюминия (27Al) 13 протонов, а нейтронов
. B) 14.
14.У атома кремния число валентных электронов равно
. C) 4.
15.Ковалентная полярная связь в молекуле
C) Аммиака.
16.Степень окисления фосфора -3 в соединении
E) PH3
17.Неэлектролит среди электролитов
А) Cu(OH)2
18.Сумма всех коэффициентов в ионном полном уравнении реакции
BaCl2 + Na2SO4 =
B) 11
19.В растворе гидроксида натрия лакмус фиолетовый
А) Синий
20.Количество вещества осадка, полученного при взаимодействии 170 г нитрата серебра и 73 г соляной кислоты
C) 1 моль
21.Вещество B в цепи превращения:S→K2S→B→SO3→H2SO4
A) Оксид серы (IV)
22.К физическим свойствам азота не относится
C) Немного тяжелее воздуха
23.Углекислый газ не взаимодействует с:
B) Оксидом серы (IV)
24.Относительная плотность оксида серы (IV) по водороду
E) 32
25.Наиболее сильный окислитель
D) Фтор
26.Более ярко выраженными металлическими свойствами обладает
E) Ba
27. В атоме кальция число протонов, нейтронов, электронов соответственно
C) 20, 20, 20
28.Сумма всех коэффициентов в схеме реакции Al + HCl AlCl3 + H2
D) 13
29.Количество вещества сероводорода, полученного при взаимодействии 32 г серы с водородом, составляет
A) 1 моль.
30.Вещество Х в ряду превращений H2S → Х→ H2SO3→CuSO3
A) SO2