Объяснение:
В 0,8 дм3 воды содержится 24,32 мг ионов магния Mg2+ и 100,2 мг ионов кальция Ca2+. Чему равна ее общая жесткость? Какую массу карбоната натрия Na2CO3 необходимо прибавить к 25 м3 такой воды для устранения ее общей жесткости?
Жёсткость воды выражается суммой миллиэквивалентов ионов Са2+ и Mg2+, содержащихся в 1 л воды (моль/л). Один миллимоль жёсткости отвечает содержанию 20,04 мг/л Ca2+ или 12,16 мг/л Mg2+.
Находим содержание Са²⁺ и Mg²⁺ в 1 л воды:
24,32 мг : 0,8 дм³ = 30,04 мг/л Са²⁺ ; 100, 2 мг: 0,8 дм³ =125,25 мг/л Mg²⁺
Ж(Са2+) = 30,04/(20,04 ·1) = 1,5 ммоль/л;
Ж(Mg2+) = 125,25/(12,16 ·1) = 10,3 ммоль/л
Общая жесткость = 1,5 + 10,3 =11,8 ммоль/л
Молярная масса эквивалента Na2CO3 = M/2 = 106/2 = 53 г/моль.
Массу карбоната натрия, необходимую для устранения жёсткости находим из формулы:
m(В) = Ж . MЭ(В) . V; m(Na2CO3) = 11,8 · 53· 25 = 15635 мг или 15,6 г
Уравнение реакции( один из вариантов):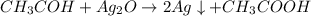
Чтобы расчитать выход продукта, нам нужно узнать сколько теоретически должно было выделиться продукта( "на бумаге").
Воспользуемся известной массой уксусного альдегида и найдём, сколько этого самого альдегида вступило в реакцию:
n( количество вещества) = m( масса) / M( молярная масса) - общая формула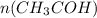 = 4,4 / 44= 0,1 моль
= 4,4 / 44= 0,1 моль
Из уравнения реакции видно, что коэффициент перед уксусным альдегидом равен коэффициенту перед уксусной кислотой, т.е. 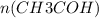 =
= 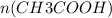 = 0,1 моль
= 0,1 моль
Теперь, пользуясь уже знакомой формулой n( количество вещества) = m( масса) / M( молярная масса), мы можем найти массу ( теоретическую) уксусной кислоты: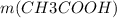 =
= 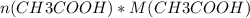 = 0,1 * 60 = 6 г.
= 0,1 * 60 = 6 г.
Выход продукта расчитываем по формуле:
w = m( практ) / m( теор) * 100% = 90%
ответ: выход продукта составил 90%.
BaO+H20 = Ba(OH)2 - реакция соединения
BaO+CO3=BaCO3 - реакция соединения