Говорю сразу. Я расписываю все действия подробно. Если тебе нужно тупо решение - под рассуждениями - действия как они должны быть на бумаге. Остальное можно не читать в таком случае.
Дано:
Уравнениие реакции: Ca + 2H2O >>> Ca(OH)2 + H2↑
пояснение к уравнению реакции при необходимости: [кальций + вода >>> гидроксид кальция + водород]
m(Ca)= 0,8 г.
Найти: V(H2)
1) Находим моль известного нам вещества (кальция) по формуле n=m/M (где m - известная нам в дано масса, а M - молярная масса кальция) - M(Ca) = 40 г/моль
n(Ca) = 0,8 / 40 = 0,02 моль
2) Сравниваем количество моль известного вещества (кальция) и того, которое нам необходимо найти (водорода). Видим, что они реагируют 1:1 (т.е. коээфициенты перед веществами в уравнении реакции отсутствуют (это всё равно что 1:1))
т.к. n(Ca)=n(H2)= 1:1 ⇒ n(H2)= 0,02 моль
3) Находим объём водорода по формуле V=n*Vm (где n - известные нам моль вещества, а Vm - всегда равно 22,4)
V(H2) = 0,02 * 22,4 = 0,448 л.
ответ: V(H2)= 0,448 л. = 448 мл.
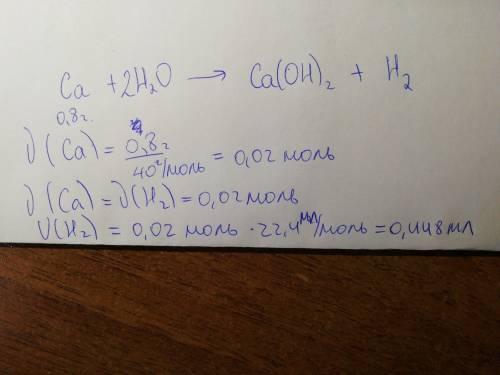
3NaOH + H3PO4 = Na3PO4 + 3H2O
n = m/M
n(NaOH) = 4/40 = 0,1 моль
n(H3PO4) = 4/98 = 0,04 моль
n(NaOH) : n(H3PO4) по условию = 0,1 : 0,04
по уравнению = 3 : 1 (см. цифры перед формулами в уравнении)
(По нашим данным в реакцию с гидроксидом натрия должно было вступить 0,1/3 = 0,033 моль ортофосфорной кислоты, а вступило 0,04. Т.к. 0,04 > 0,033, значит кислота находилась в избытке. Будем считать по гидроксиду натрия).
n(NaOH) : n(Na3PO4) = 3 :1
n(Na3PO4) = 0,1/3 = 0,033 моль
m(Na3PO4) = 0,033 * 164 = 5,412 г
ответ: 5,412 г
Поставьте как лучший
C2H4+Cl2->C2H4Cl2