Объяснение:
Mr(H₂SO₄)=2Ar(H)+Ar(S)+4Ar(O) (записуємо відносну атомну масу елементів і вказуємо попереду елемента індекси).
Mr(H₂SO₄)=2+32+4x16=2+32+65=98 (знаходимо в ПСХЕ атомні маси, множимо на індекс і визначаємо молекулярну масу ).
Визначаємо масові частки елементів, для цього ділимо відносну масу елемента на молекулярну масу:
ω(H)=2Ar(H)÷Mr(H₂SO₄)=2÷98=0,0204
ω%(H)=ω(H)×100%=0,0204×100%=2,04
ω(S)=Ar(S)÷Mr(H₂SO₄)=32÷98=0,3265
ω%(S)=ω(S)×100%=0,3235×100%=32,65%
ω(O)=4Ar(O)÷Mr(H₂SO₄)=64÷98=0,6531
ω%(O)=ω(O)×100%=0,6531×100%=65,31%
Объяснение:
n - кол-во вещества
V - объем
Что бы найти количество вещества, можно сделать пропорцию. 25Г надо поставить сверху CaCO3, а снизу его молярную массу, так как Если 25 / 100, то получится количество вещества, следовательно массу СаО, берем как Х, а молярную массу мы и можем найти благодаря таблице Менделеева. В результате,у нас получилась такая пропорция, 25 / 100 = Х/56. Так как X неизвестен, мы 56 умножаем на 25 и делим на 100. Благодаря этой пропорции, мы получаем массу СаО. Если, мы знаем массу, то мы можем найти "n".
Чтобы найти количество вещества, надо массу поделить на молярную массу (на фотографии показано решение). В результате чего получится, 0,25 моль.
В этой задаче, чтобы найти объем мы должны количество вещества умножить на Vm (Vm всегда равен 22.4 л). Количество вещества углекислого газа мы знаем, так как, Если количество вещества оксида кальция (СаО) равен 0,25 то и количество вещества углекислого газа (СО2) будeт равно 0,25, ведь реакция полностью. Из-за этого мы спокойно можем выбрать количество вещества оксида кальция и для углекислого газа.
Надеюсь, я смогла объяснить.
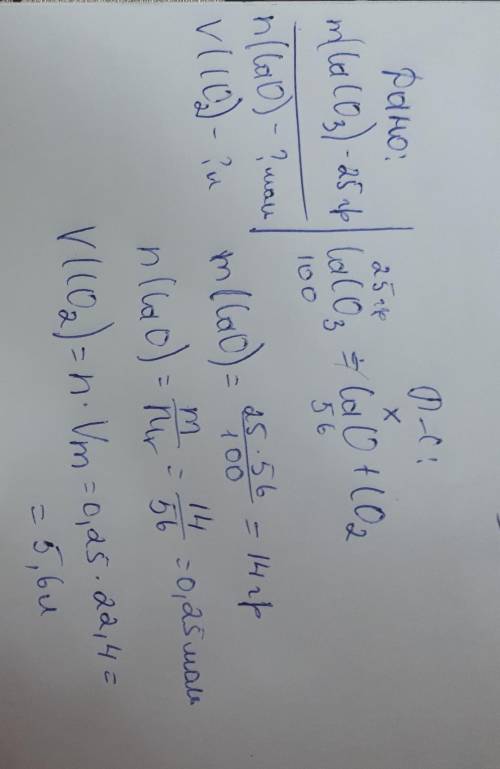
2.Атомная кристаллическая решётка
3.Элементарный фосфор существует в виде нескольких устойчивых аллотропических модификаций. Все возможные модификации фосфора пока (2014 г.) до конца не изучены. Традиционно различают четыре его модификации: белый, красный, чёрный и металлический фосфор. Иногда их ещё называют главными аллотропными модификациями, подразумевая при этом, что все остальные описываемые модификации являются смесью этих четырёх. При стандартных условиях устойчивы только три аллотропических модификации фосфора (например, белый фосфор термодинамически неустойчив (квазистационарное состояние) и переходит со временем при нормальных условиях в красный фосфор). В условиях сверхвысоких давлений термодинамически устойчива металлическая форма элемента.