Энтропия — в естественных науках мера беспорядка системы, состоящей из многих элементов. В частности, в статистической физике — мера вероятности осуществления какого-либо макроскопического состояния; в теории информации — мера неопределённости какого-либо опыта (испытания), который может иметь разные исходы, а значит, и количество информации; в исторической науке, для экспликации феномена альтернативности истории (инвариантности ивариативности исторического процесса).
Энтальпия, также тепловая функция и теплосодержание —термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.Проще говоря, энтальпия — это та энергия, которая доступна для преобразования в теплоту при определенных температуре и давлении.
Дано:
m (бутена) = 100 %;
галоген (обозначим его Г);
m (после р.-ции) = 167,86 %.
Найти:
галоген (Г) — ?
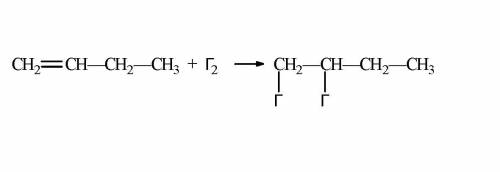
1. Сначала напишем реакцию в общем виде (прикреплена ниже на фото).
2. Затем посчитаем молярную массу бутена. Берём значения из таблицы Менделеева.
M (C₄H₈) = 4 · 12 + 8 = 56 (г/моль).
3. Массу бутена примем за 100%, а массу галогенпроизводного будем считать за 167,86%.
Таким образом мы найдём молярную массу галогенпроизводного.
56 г/моль — 100 %
x г/моль — 167,86 %
x ≈ 94 (г/моль).
4. По уравнению реакции видим, что количество углеродов и водородов не поменялось, но теперь "висят" два радикала галогена.
Значит, от массы галогенпроизводного отнимем "бутен", чтобы у нас остались только галогены, а так как их два, разделим на 2 и узнаем молярную массу искомого галогена.
M (Г) = (94 г/моль – 56 г/моль) ÷ 2 = 19 (г/моль).
Смотрим по таблице Менделеева... это фтор (F)!
ответ: фтор (F).