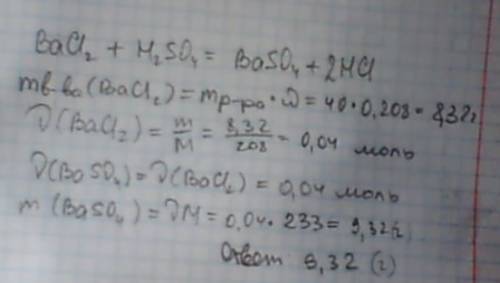
Відповідь:
3. m(раствора) =298.4 г
4. m(раствора)=98,67 g
Пояснення:
Задача 3. Дано: w(HNO₃)=0.15 . m(Cr₂O₃)=18 gI. Запишем реакцию:
6 HNO₃ + Cr₂O₃ → 3 H₂O + 2 Cr(NO₃)₃
С реакции видно, что соотношение количества между реагентами, как 6:1. Тоесть, 6n(HNO₃)=n(Cr₂O₃)
II. Запишем формулы // Проведем вычисления:
n(E)=m(E)/Mr(E)
m(E)=n(E)*Mr(E)
w(E)=m(E)/m(раствора)
Запишем соотношение за количеством вещества:
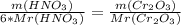
m(HNO₃)=m(Cr₂O₃)*6Mr(HNO₃)/Mr(Cr₂O₃)
m(HNO₃)=18*6*63/152=44.76 g
Подставляем эту массу формулу массовой доли:
0.15=44.76/m(раствора)
m(раствора) = 44.76/0.15=298.4 г
Задача 4. w(Mg(NO₃)₂)=15% w(NaOH)=8% m(раствора NaOH)=100gI. Запишем реакцию:
Mg(NO₃)₂ + 2 NaOH → 2 NaNO₃ + Mg(OH)₂ ↓
С реакции видно, что соотношение количества между реагентами, как 1:2. Тоесть, нужно 1х моль Mg(NO₃)₂ и 2x моль NaOH.
II.Запишем формулы // Проведем вычисления:
n(E)=m(E)/Mr(E)
m(E)=n(E)*Mr(E)
w(E)=m(E)/m(раствора) · 100%
m(E)=w(E)*m(розчину) / 100%
m(NaOH)=100*8/100=8 g
n(NaOH)=8/40=0.2 моль
n(Mg(NO₃)₂)=0.2/2=0.1 моль
m(Mg(NO₃)₂)=0.1*148=14.8 g
15 = 14.8 · 100% / m(раствора)
m(раствора)=14.8 · 100% / 15=98,67 g
*Поставьте лучшее
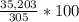 % = 11,54%
% = 11,54% 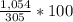 % = 0,35%
% = 0,35%