V=m/M;
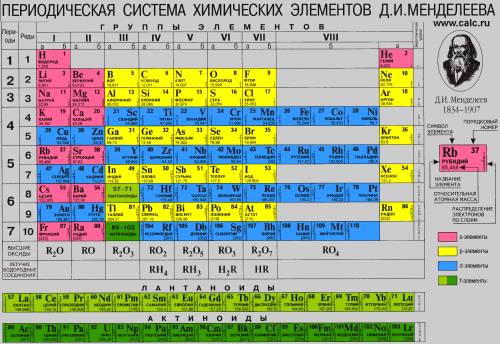
m=V*M; - количество вещества дано по условию, М(молярная масса) находится из таблицы Менделеева как сумма атомных масс элементов:
1) m(CaCO₃)=V*M=2*(40+12+48)=2*100=200 г;
2) m(NaCl)=V*M=5*(23+35,5)=5*58,5=292,5 г;
3) m(CO₂)=V*M=0,25*(12+32)=0,25*44=11 г.
m(в-ва)=M*V
где, M - молярная масса, а V(ню)-массовая доля вещества
V(CaCO3)=100г/моль
m(CaCO3)=2*100=200грамм
V(NaCl)=58,5г/моль
m(NaCl)=5*58,5=292,5грамм
V(CO2)=44г/моль
m(CO2)=0,25* 44=11грамм