Природные органические вещества и их превращения лежат в основе явлений Жизни. Поэтому органическая химия является химическим фундаментом биологической химии и молекулярной биологии - наук, изучающих процессы, происходящие в клетках организмов на молекулярном уровне. Исследования в этой области позволяют глубже понять суть явлений живой природы.
Множество синтетических органических соединений производится промышленностью для использования в самых разных отраслях человеческой деятельности.
Это - нефтепродукты, горючее для различных двигателей, полимерные материалы (каучуки, пластмассы, волокна, пленки, лаки, клеи и т.д.), поверхностно-активные вещества, красители, средства защиты растений, лекарственные препараты, вкусовые и парфюмерные вещества и т.п. Без знания основ органической химии современный человек не экологически грамотно использовать все эти продукты цивилизации.
Объяснение:
1) Ar 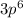 N = 3 L = 1 Ml = 1 Ms = -½
N = 3 L = 1 Ml = 1 Ms = -½
2) Na 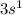 N = 3 L = 0 Ml = 0 Ms = +½
N = 3 L = 0 Ml = 0 Ms = +½
3) Mg 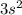 N = 3 L = 0 Ml = 0 Ms = -½
N = 3 L = 0 Ml = 0 Ms = -½
4) Al 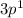 N = 3 L = 1 Ml = -1 Ms = +½
N = 3 L = 1 Ml = -1 Ms = +½
Объяснение:
Главное квантовое число N характеризует энергетический уровень, другими словами это размер энергетического уровня, чем больше число N - тем больше радиус, на котором находятся электроны.
Орбитальное квантовое число L обозначает форму той области, в которой может находится электрон, число L имеет значения s (L=0),p (L=1), d (L=2),f (L=3) и также называется энергетической оболочкой или энергетическим подуровнем.
На каждой орбитали находится «2·L + 1» орбиталей, магнитное квантовое число Ml обозначает орбиталь, на котором находится электрон. Ml может принимать значения ±L.
И последнее квантовое число - спин, он принимает два значения: +½ и -½, обозначающий соответственно прямое и обратное вращение электрона.
Квантовые числа элемента, или квантовые числа электрона - это четыре квантовых числа, характеризующих состояние внешнего электрона в атоме.
₊₁₄ Si - 3-й период, главная подгруппа IV группа;
2.3.
Внимание! Текст вопроса №2 нарушен. Его удалось восстановить по кусочкам, но есть вероятность неправильного восстановления!
Восстановленный текст вопроса: строение внешнего энергетического уровня 3s² 3p³ соответствует атому:
1. магния 2. серы 3. фосфора 4. хлора
ответ: 3. Электронная конфигурация фосфора ₊₁₅P 1s² 2s² 2p⁶ 3s² 3p³
3. 3. сера
В одном периоде чем правее элемент (не считая инертных газов), тем слабее его металлические свойства и тем сильнее его неметаллические свойства.
4. 4. ЭО₃
Элемент Э с зарядом ядра +16 - это сера ₊₁₆S. Высший оксид серы - SO₃
5. 2. кислотный
Элемент с номером 7 - это азот ₊₇N. Высший оксид азота - N₂O₅. Это кислотный оксид. С водой он образует азотную кислоту:
N₂O₅ + H₂O = 2 HNO₃
6. 1. бария
Основные свойства усиливаются в группе с ростом атомного номера (другими словами, чем ниже элемент в группе, тем сильнее его основные свойства ). Самый большой атомный номер у бария - 56.
7. 1. CuO + H2 = Cu + H2O
Только в этой реакции медь от степени окисления +2 восстанавливается до степени окисления 0 (до металлической меди)
8.4.
Внимание! Текст вопроса №8 нарушен. Его удалось восстановить по кусочкам, но есть вероятность неправильного восстановления!
Восстановленный текст вопроса: сокращенное ионное уравнение реакции Ba²⁺ + SO₄²⁻ = BaSO4↓ соответствует взаимодействию:
1. бария и раствора серной кислоты;
2. оксида бария и соляной кислоты;
3. оксида бария и раствора серной
кислоты;
4. хлорида бария и раствора серной
кислоты.
ответ: 4.
Вариант 1 не подходит, поскольку это не реакция ионного обмена, а окислительно-восстановительная реакция. Металлический барий Ba окисляется до катионов бария Ba²⁺ ионами водорода H⁺ из серной кислоты H₂SO₄. В ходе этой реакции сульфат бария BaSO₄ будет образовываться:
Ba + H₂SO₄ = BaSO₄↓ + H₂↑ ,
или в ионном виде:
Ba + 2 H⁺ + SO₄²⁻ = BaSO₄↓ + H₂↑ ,
но это уравнение не соответствует ионному уравнению из условия задачи.
Вариант 2 не подходит, потому что среди реагентов нет сульфат-ионов.
Вариант 3 почти подходит - это обменная реакция, и сульфат бария будет в ходе нее образовываться:
BaO + H₂SO₄ = BaSO₄↓ + H₂O
или в ионном виде:
BaO + 2 H⁺ + SO₄²⁻ = BaSO₄↓ + H₂O
однако как и в первом варианте, это уравнение не соответствует данному в условии.
Вариант 4 подходит:
BaCl₂ + H₂SO₄ = BaSO₄↓ + 2 HCl
в ионном виде
Ba²⁺ + 2 Cl⁻ + 2 H⁺ + SO₄²⁻ = BaSO₄↓ + 2 H⁺ + 2 Cl⁻
или в краткой форме:
Ba²⁺ + SO₄²⁻ = BaSO₄↓
Последнее уравнение совпадает с данным в условии/
9. 1. HCl
Гидроксид кальция, как и все основания, реагирует с кислотами и кислотными оксидами. Из списка вариантов HCl - единственная кислота, а кислотных оксидов в нем вовсе нет.
10. 4. углерод
Только углерод подходит под схему превращений:
Э → ЭО₂ → Н₂ЭО₃
Варианты алюминия и магния отвергаются на стадии получение оксида: для их оксидов Al₂O₃ и MgO формула ЭО₂ не подходит.
Азот образует оксид NO₂, но азотная кислота HNO₃ не соответствует формуле H₂ЭО₃
Часть Б..
11.
Элемент №3 - литий ₊₃Li
Элемент №9 - фтор ₊₉F
Значит, речь идет о реакции растворов гидроксида лития LiOH и фтороводорода HF:
LiOH + HF = LiF + H₂O
LiOH - гидроксид лития
HF - фтороводород (его водный раствор - фтороводородная или плавиковая кислота)
LiF - фторид лития
H₂O - вода
Это реакция обмена. В данном случае ее еще называют реакцией нейтрализации (нейтрализации кислоты щелочью)
12.
BaO → Ba(OH)2 → BaCO3 → BaCl2,
составьте уравнения реакций в молекулярном виде.
Для превращения No3 запишите полное
и сокращенное ионные уравнения.
1) BaO + H₂O = Ba(OH)₂
2) Ba(OH)₂ + CO₂ = BaCO₃↓ + H₂O
3) BaCO₃↓ + H₂SO₄ = BaSO₄↓ + H₂O + CO₂↑
Полное ионное уравнение:
BaCO₃↓ + 2 H⁺ + SO₄²⁻ = BaSO₄↓ + H₂O + CO₂↑
Сокращать нечего, так что это одновременно и краткое ионное уравнение.
13.
По уравнению реакции 2Mg + O2 = 2MgO рассчитайте объем кислорода
(н.у.), необходимого для полного сгорания 1,2 г магния
M(Mg) = 24,3 г/моль
По уравнению на 2 моль (2*24,3 г) магния нужно 22,4 л кислорода:
Соответственно, на 1,2 г магния нужно х л кислорода.
2 Mg + O₂ = 2 MgO
2*24,3 г 22,4 л
1,2 г х л
х = 1,2 г*22,4 л /(2*24,3 г) = 0,55 л.
ответ: 0,55 л O₂