Это уравнение как для ОВР не простое, так как степень окисления железа в 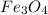 равна
равна 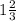 :
:
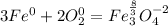
Так что рассмотрим сложный оксид 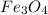 как сумму двух
как сумму двух 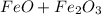
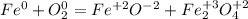
Рассмотрим процессы

Так как количество принятых электронов равно количеству отданных, то перед кислородом идет коэффициент 2, а перед вторым уравнением тоже идет коэффициент 2:
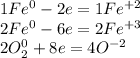
Получается суммарно 3 атома железа отдали 8 электронов и 4 атома кислорода приняли 8 электронов
Кислород - окислитель, железо - восстановитель
Тогда суммарный коэффициент перед железом 1 + 2 = 3, а перед кислородом 2, тогда:

δt = 1 ч = 3600 с
i = 0,268 a
v(h2) = 11,2 мл = 11,2*10^(-3) л
f = 965480 кл/моль
сульфат кадмия cdso4 – соль, образованная слабым основанием cd(oh)2 и сильной кислотой h2so4 которая в водном растворе гидролизуется по катиону.
2cdso4 + 2н2о = (cdoh)2so4 + h2so4
cd (2+) + н2о = cdoh(+) + н (+) (ph < 7 – среда кислая)
анодный процесс
при электролизе растворов солей, содержащих в своем составе сульфат-ион so4(2-) на аноде происходит окисление воды с выделением свободного кислорода.
анод (+) 2н2о – 4е = 4н (+) + о2↑ (рн < 7)
катодный процесс.
поскольку кадмий в ряду напряжений стоит после алюминия и до водорода, то на катоде одновременно будут протекать два процесса – восстановление ионов cd(2+) и восстановление ионов водорода н (+) (поскольку среда кислая)
cd(2+) + 2e = cd↓
2h(+) + 2e = h2↑
суммарная реакция на катоде
катод cd(2+) + 2h(+) + 4e = cd + h2↑
тогда процессы окисления – восстановления, протекающие при электролизе раствора сульфата кадмия cdso4
2н2о – 4е = 4н (+) + о2↑ | 1 - окисление
cd(2+) + 2h(+) + 4e = cd + h2↑ | 1 – восстановление
суммарно
cd(2+) + 2h(+) + 2н2о = cd + h2↑ + 4н (+) + о2↑
после подобных
cd(2+) + 2н2о = cd + h2↑ + 2н (+) + о2↑
уравнение реакции в молекулярном виде
cdso4 + 2н2о = cd + h2↑ + н2so4 + о2↑
поскольку на катоде одновременно протекают два процесса – восстановление ионов cd(2+) и восстановление ионов водорода h(+), то суммарное количество электричества, затраченное на восстановление ионов кадмия и водорода, будет равно количеству электричества, прошедшего через электролит.
чтобы найти выход по току для кадмия найдем выход по току для водорода.
эквивалентный объем водорода найдем как эквивалентный объем двухатомного газа при н. у.
vэкв (н2) = vm/(2*z(н2)) = 22,4/(2*1) = 11,2 л
vm = 22,4 л/моль – молярный объем при н. у.
z(н2) = 1 – число связей в молекуле н2
по первому закону фарадея найдем количество электричества, затраченное на восстановление водорода объемом 11,2 мл.
v(h2) = vэкв (н2)*q(h2)/f
q(h2) = v(h2)*f/vэкв (н2) = 11,2*10^(-3)*96480/11,2 = 96,48 кл
суммарное количество электричества, прошедшее через электролит.
q = i*δt = 0,268*3600 = 964,8 кл
количество электричества, затраченное на восстановление ионов кадмия.
q(cd) = q – q(h2) = 964,8 – 96,48 = 868,32 кл
выход по току для кадмия
η(cd) = [q(cd)/q]*100% = [868,32/964,8]*100% = 90%
формула оксида в общем виде MeO
запишем уравнения:
2Me+O₂=2MeO
MeO+H₂O=Me(OH)₂
5г xг
2Me+O₂=2MeO
2 моль 2моль
Ar(Me) Ar(Me)+16
2Ar(Me) 2Ar(Me)+32
m(MeO)= 5*(2Ar(Me)+32)\ 2Ar(Me) г
хг 9,25г
MeO +H₂O = Me(OH)₂
1 моль 1 моль
Ar(Me)+16 Ar(Me)+34
m(MeO)=(Ar(Me)+16)*9,25\Ar(Me)+34г
10Ar(Me)+160\2Ar(Me) = 9,25Ar(Me)+148\Ar(Me)+34
2(5Ar(Me)+80)\2Ar(Me)= 9,25Ar(Me)+148\Ar(Me)+34
5Ar(Me)+80\Ar(Me)= 9,25Ar(Me)+148\Ar(Me)+34
(5Ar(Me)+80)*(Ar(Me)+34)=Ar(Me)*9,25Ar(Me)+148
5(Ar(Me))²+170Ar(Me)+80Ar(Me)+2720=9,25(Ar(Me))²+148Ar(Me)
5(Ar(Me))²+250Ar(Me)+2720=9,25(Ar(Me))²+148Ar(Me)
-4,25(Ar(Me))²+102Ar(Me)+2720=0
17(Ar(Me))²-408Ar(Me)-10880=0
Ar(Me)²-24Ar(Me)-640=0
D1=144+640=784
Ar(Me)1=12+28
Ar(Me)2=12-28
Ar(Me)1=40
Ar(Me)2=-16 <0 не удовлетворяет условие Ar(Me)>0
Значит Ar(Me)=40
Значит искомый металл кальций Ca
ответ: Сa - кальций