5 м в кубе х м в кубе
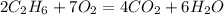
2 объема 7 объемов
1.Согласно уравнения и закона объемных отношений газов найдем объем кислорода:
для полного сжигания 2 объемов этана необходимо 7 объемов кислорода, а
для --//--//-- 5 м в кубе________________х м в кубе, откуда
х=5*7/2=17,5 м в кубе
2. Учитывая,что оббъемная доля кислорода в воздухе всего 21%,тогда:
17,5 м в кубе - это 21%, а
у м в кубе воздуха - 100%, откуда у=17,5*100/21=приблизительно 83 м в кубе
А теперь попробуй решить задание сама,вторая задача подобная(один к одному), а уравнение реакции будет такое^
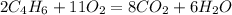
Получение основных оксидов:
1. Окисление металлов при нагревании в атмосфере кислорода:
2Mg + О2 = 2МgО,
2Сu + О2 = 2СuО.
Этот метод практически неприменим для щелочных металлов, которые при окислении обычно дают пероксиды, поэтому оксиды Na2О, К2О крайне труднодоступны.
2. Обжиг сульфидов:
2CuS + ЗО2 = 2СuО + 2SО2,
4FeS2 + 11О2 = 2Fе2О3 + 8SО2.
Метод неприменим для сульфидов активных металлов, окисляющихся до сульфатов.
3. Разложение гидроксидов:
Cu(OH)2 = CuO + H2O
Этим методом нельзя получить оксиды щелочных металлов.
4. Разложение солей кислородсодержащих кислот:
BaCO3 = BaO + CO2
2Рb(NО3)2 = 2PbО + 4NO2+O2
4FеSО4 = 2Fe2O3 + 4SO4 + O2
2NaOH + H2SO4 = Na2SO4 + 2H2O
80 98 142
n(NaOH) = 20/40 = 0.5 моль
n(H2SO4) = 30/98 = 0.3 моль
Считаем по недостатку (по кислоте):
m(Na2SO4) = 142 * 30 / 98 = 43.5г