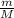 , где ν (ню) - количество вещества, m - масса вещества, M - молярная масса. Таким образом, чтобы вычислить любое из неизвестных, надо подставить два других. В нашем случае неизвестно количество вещества - подставляем в формулу вместо m 5,1 (из условия), а вместо M - 34 (Молярную массу можно найти по таблице Мендлеева - она равна сумме масс всех атомов в молекуле. Два атома серы весят по 16 г/моль = 32, а один атом водорода весит 2 г/моль. Всё вместе даёт 34)
, где ν (ню) - количество вещества, m - масса вещества, M - молярная масса. Таким образом, чтобы вычислить любое из неизвестных, надо подставить два других. В нашем случае неизвестно количество вещества - подставляем в формулу вместо m 5,1 (из условия), а вместо M - 34 (Молярную массу можно найти по таблице Мендлеева - она равна сумме масс всех атомов в молекуле. Два атома серы весят по 16 г/моль = 32, а один атом водорода весит 2 г/моль. Всё вместе даёт 34)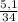
n(NaOH) = m/M = 32/40 = 0,8 моль
n(H2SO4) = n(NaOH) / 2 = 0,8 : 2 = 0,4 моль
m(H2SO4) = M*n = 98 * 0,4 = 39,2 г
ω = m в-ва/m р-ра = 39,2 / (39,2 + m(H2O)) = 0,1 | * (39,2 + m(H2O))
39,2 = 3,92 + 0,1m(H2O)
0,1m(H2O) = 35,28 | * 10
m(H2O) = 352,8 г
m(р-ра H2SO4) = m(H2O) + m(H2SO4) = 39,2 + 352,8 = 392 г
V(р-ра H2SO4) = m/p = 392 / 1,07 = 366,36 cм³
ответ: Объём раствора 10% H2SO4 равен 366,36 cм³.