ZnSO4+2KOH=Zn(OH)2(ОСАДОК) +K2SO4
Zn2+ + SO4 2- + 2K+ + 2OH- = Zn(OH)2(ОСАДОК) + 2K+ + SO4 2-
Zn2+ +2OH-= Zn(OH)2(ОСАДОК)
Na2CO3 + 2HNO3= 2NaNO3 + H20 + CO2(ГАЗ)
2Na+ + CO3- + 2H+ + 2NO3- = 2Na+ +2NO3- + H20 + CO2(ГАЗ)
CO3- + 2H+=H20 + CO2(ГАЗ)
СuO + 2HCL = НЕТ ИОННОЙ РЕАКЦИИ ТАК КАК ОКСИДЫ НЕ ЯВЛЯЮТСЯ ЭЛЕКТРОЛИТАМИ..
1. При прибавлении к раствору цитрата избытка известковой воды на холоду осадка не образуется. При нагревании же выпадает хлопьевидный осадок цитрата калия, при охлаждении (в закрытой колбе) вновь растворяющийся.
2. Нагревают 5 мл 1%-ного раствора лимонной кислоты с 1 мл реактива Дениже (5 г окиси ртути растворяют в смеси 20 мл концентрированной серной кислоты и 100 мл воды при нагревании до кипения) и прибавляют несколько капель 2%-ного раствора пер-манганата калия. Жидкость обесцвечивается и выпадает белый кристаллический осадок:
Промытый осадок растворяется в растворе хлорида натрия с образованием хлорида ртути и ацетон-дикарбоновой кислоты, которая с хлоридом железа дает малиново-красное окрашивание. 3. Реакция образования пентабромацетона
К водному раствору лимонной кислоты или цитрата в очень разбавленной серной или азотной кислоте (но не соляной) прибавляют
2-5 капель 0,1 н. раствора перманганата калия и нагревают в течение непродолжительного времени до 30-40° (только не кипятить!). Как только раствор побуреет или помутнеет от незначительного выделения двуокиси марганца, прибавляют 1-2 капли раствора ок-салата аммония и 1 мл 10%-ной серной кислоты, при этом жидкость становится прозрачной. Затем прибавляют несколько капель бромной воды. При этом выделяется кристаллический осадок пента-бромацетона.1
4.Глюкоза даёт синее окрашивание с свежеприготовленным Сu(OH)2. Даёт реакцию серебрянного зеркала с Ag(NH3)2OH/
 моль
моль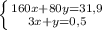
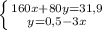

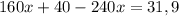

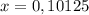 моль (это количество вещества Fe₂O₃)
моль (это количество вещества Fe₂O₃)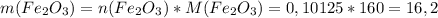 г
г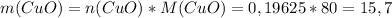 г
г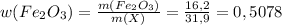 или 50,78% (где m(X) - это масса смеси)
или 50,78% (где m(X) - это масса смеси)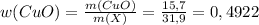 или 49,22%
или 49,22%
1)ZnSO4 + 2 KOH = K2SO4 + Zn(OH)2
2)Na2CO3 + 2 HNO3 = H2CO3 + 2 NaNO3