Cu - медь.
Объяснение:
При разложении гидроксида двухвалентного металла массой 19.6 г, образуется оксид двухвалентного металла массой 16 г. Определите металл. Решите с уравнения реакции.
Металл обозначим как - «Me», тогда общая формула будет : Me(OH)2, так как OH-группа является одновалентной.
Схема разложения: Me(OH)2 —> MeO + H2O
Дано:
m(MeOH)2 = 19.6 г
m(MeO) = 16 г.
m(H2O) = 19.6 - 16 = 3.6 грамм
Помним, что сумма реагентов и образующихся продуктов должна быть равной !
И так, нам известно, что воды образуется 3.6 грамм по задаче, а по реакции 18 грамм, из этого следует, что:
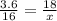
x= 80
80 грамм молекулярная масса оксида двухвалентного металла (MeO)
80-16(кислород в составе MeO) = 64 г
64 г это атомная масса Меди.
Если будут вопросы, отвечу с удовольствием в комментариях.
Электролит для гальванического серебрения состоит из следующих компонентов: хлористое серебро — 10— 15 г, желтая кровяная соль (железоцианистый калий) — 15—35 г, кальцинированная сода — 15—35 г, вода (желательно дистиллированная) — 1000 г. Температура работы электролита — 18—20град. С, плотность тока — 0,1 А/дм2. Как анод используются графитовые пластины. Каждый компонент входящий в состав электролита растворяют отдельно в кипящей воде. Хлористое серебро растворяют в темном месте. Растворы желтой кровяной соли и кальцинированной соды вливают в раствор хлористого серебра и кипятят вместе в течение 1,5—2 ч, после чего все фильтруют. Готовый электролит имеет светло-желтый оттенок и не включает в себя осадок.