І.Выберите три верных ответа. С водородом реагируют оба вещества в наборах: 1,3,5
ІІ.1.Сначала определим массу соли в первоначальном растворе:
m1(соли)=m1(раствора)*w1(соли)=100*0,15=15 г
2.Узнаем массу соли в новом растворе,сложив уже имеющуюся(ту,что только что определили) и добавленную:
m(соли)=m1(соли)+m2(соли)=15+50=65 г
3.Вычислим массу нового раствора,сложив массу первоначального раствора с массой добавленной соли:
m2(раствора)=m1(раствора)+m2(соли)=100+50=150 г
4. Отнеся массу соли в новом растворе к массе этого раствора,получим массовую долю соли в новом растворе:
w2(соли)=m(соли)/m2(раствора)=65/150=0,43 или 43%
ІІІ.
+7 -1 +2 0
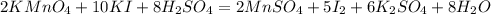
+7 +2
Mn + 5e = Mn|2| окислитель(восстановление)
-1 0
2I - 2e = I2 |5| восстановитель(окисление)
IV.
4488 г х л
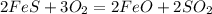
176 г 44,8 л
1. Определим чистую массу сульфида в образце:
5610 г образца - это 100%,
у г_______________80%, откуда у=5610*80/100=4488 г
2. По этой массе,подставив ее в уравнение реакции,определим объем сернистого газа:
при взаимодействии 176 г сульфида образуется 44,8 л сернистого газа, а
при --//--//-- 4488 г__________________Х л, откуда=
х=4488*44,8/176=1142 л или 1,142 м в кубе
В оксиде железа III железо имеет степень окисления +3, следовательно, он будет растворяться в кислотах
Fe2O3 + 6HCl —> 2FeCl3 + 3H2O
Гидроксиды металлов образуются при взаимодействии их солей с щелочами
FeCl3 + 3NaOH —> Fe(OH)3 + 3NaCl
Более активные металлы могут восстанавливать менее активные
2Fe(OH)3 + 2Al —> 2Fe + Al2O3 + 3H2O
Железо растворяется в разбавленной серной кислоте с образованием сульфата железа 2. Если бы кислота была концентрированная, то образовался бы хлорид железа 3
Fe + H2SO4 —> FeSO4 + H2
FeSO4 + 2NaOH —> Fe(OH)2 + Na2SO4
Во влажном воздухе гидроксид железа 2 окисляется кислородом
4Fe(OH)2 + O2 + 2H2O —> 4Fe(OH)3
3) BaCl2 +
42. В растворе какого вещества есть хлорид-анион:
2) HCl
43. Наличие хлорид-аниона в растворе можно определить с
3) нитрата серебра
44. При растворении в воде катионы металлов образуют все вещества группы:
2) Al(NO3)3, Ba(OH)2, Fe2(SO4)3
45. В растворе одновременно могут присутствовать ионы:
4) Zn2+ и Cl-
46. В растворе не могут одновременно находиться вещества:
4) Na2CO3 и CaCl2
47. Образование воды возможно при взаимодействии растворов веществ:
2) H3PO4 и Ba(OH)2
48. Сокращенное ионное уравнение Cu2+ + 2 OH- = Cu(OH)2 соответствует реакции между:
3) CuCl2 и KOH
49. Сущность реакции обмена между раствором хлорида бария и раствором серной кислоты можно выразить сокращенным ионным уравнением:
4) Ba2+ + SO42- = BaSO4
50. Соль и вода образуются при взаимодействии:
4) азотной кислоты и гидроксида калия
51. Практически осуществима реакция между:
1) раствором серной кислоты и гидроксидом алюминия
52. Для распознавания солей Na2CO3 и Na2SiO3 можно использовать:
4) соляную кислоту
53. Хлорид бария не реагирует с :
5) СuO
54. Осадок голубого цвета получится в результате реакции между:
4) NaOH и CuSO4
55. Сокращенное ионное уравнение CO32- + 2H+ = H2O + CO2 соответствует реакции между:
3) K2CO3 и HCl
56. Сущность реакции обмена между раствором нитрата серебра и раствором хлорида натрия можно выразить сокращенным ионным уравнением:
3) Ag++Cl-=AgCl
57. При взаимодействии каких ионов в растворе не образуется газ?
5) Cu2+ и OH-
58. Раствор сульфата меди(II) не реагирует с раствором
4) фосфата аммония
59. При взаимодействии каких ионов в растворе не образуется осадок?
3) H+ u S2- +
60. Какое из указанных веществ взаимодействует с раствором фосфата натрия?
3) нитрат серебра