смотри если что непонятно написано спрашивай
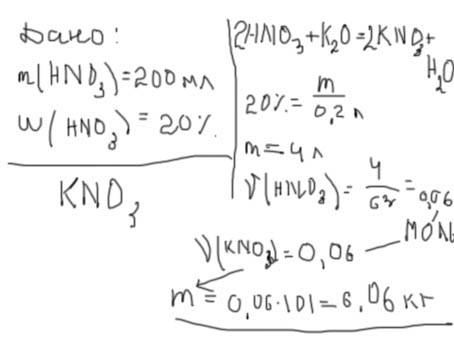
Составим уравнение реакции:
36г Хл
2Mg + O2 = 2MgO
2*24 г/моль 22,4 л/моль
Найдем молярную массу массу магния:
М (Mg) = 24 г/моль.
Составляем пропорцию:
( Х / 22,4 ) = ( 36 / 2*24 )
Из пропорции находим Х :
Х = ( 22,4 * 36 ) / ( 2 * 24 ) = 16,8л - объем чистого кислорода в воздухе.
Теперь найдем объем воздуха необходимый для сжигания 36г магния :
0,21 - 16,8л
1 - Y л .
Из пропорции находим Y :
Y = 16,8 / 0,21 = 80л - необходимый объем воздуха для сжигания 36г магния.
Дано:
V(HNO3)=20мл
W(HNO3)=20%=0.2
Плотность(ро)=1,115г/мл
m(KNO3)=?
m(р-раHNO3)= Плотность(ро)*V=1.115*20=22.3 г
m(HNO3)=22.3*0.2=4.46 г
KCL+HNO3=KNO3+HCL
4.46 г=х г
63 г= 101 г
х=4,46*101/63=7,15 г