Метанол- жидкость наливается в рюмочку, из тонкой медной (обязательно) проволочки сворачивается спиралька, нагревается на зажигалке докрасна и погружается в жидкость, которую тут же с поверхности надо понюхать. Запах формалина выдаст метанол.(Если метанол в чистом виде, то легче всего определить по температуре кипения)
Метаналь- реакцией серебряного зеркала
Уксусная кислота - с индикаторов.Лакмус в кислой среде становится красным, фенолфталеин свою окраску не меняет, а метиловый оранжевый приобретает насыщенный розово-красный цвет.
муравьиная кислота - также индикаторами(В Вашем случае реакция серебряного зеркала)
Этанол - Возьмите пробирку и поместите в нее 1-2 кристаллика йода. Добавьте исследуемое вещество, а именно этиловый спирт или этанол в количестве 1 мл. Осторожно нагрейте раствор на водяной бане, после чего добавьте 2 мл гидроксида натрия. Оставьте полученную смесь для остывания. Через некоторое время появляется запах йодоформа, а также наблюдается выделение его в виде взвеси. Если концентрация спирта изначально была высокой, то выпадает желтый осадок. Характерные признаки могут проявиться не сразу, а спустя лишь несколько часов или даже сутки.
Этиленгликоль - Распознать этиленгликоль можно с реакции с гидроксидом меди (II). Реакция даёт ярко синий комплекс.
Немного теории для начала.
Массовую долю элемента в веществе рассчитывают по формуле:
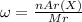 (*), здесь
(*), здесь 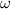 - массовая доля, nAr(x) - атомная масса элемента, n - когда в веществе присутствует несколько атомов данного элемента, например H2SO4 - тут два водорода, значит будет - 2Ar(H), ну и Mr - молекулярная масса вещества, ее рассчитывают с периодической системы, складывая атомные массы, учитывая количество атомов элемента в веществе. Ну и для Mg(OH)2
- массовая доля, nAr(x) - атомная масса элемента, n - когда в веществе присутствует несколько атомов данного элемента, например H2SO4 - тут два водорода, значит будет - 2Ar(H), ну и Mr - молекулярная масса вещества, ее рассчитывают с периодической системы, складывая атомные массы, учитывая количество атомов элемента в веществе. Ну и для Mg(OH)2
- Считаем молекулярну массу:
Mr(Mg(OH)2) = Ar(Mg) + 2Ar(O) + 2Ar(H) = 24 + 32 + 2 = 58
- Теперь подставляем данные в формулу (*):
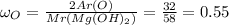 если в процентах, то
если в процентах, то
55%
3ZnSO4+2K3PO4=Zn3(PO4)2(в осадок)+3K2SO4
3Zn(2+)+3SO4(2-) +6K+ +2PO4(3-)=Zn3(PO4)2+6K+ +3SO4(2-)
3Zn(2+)+2PO4(3-)=Zn3(PO4)2