1) По определению массовая доля показывает массу растворенного вещества в 100 г раствора. Отсюда узнаем массу CuCl₂, которая будет содержаться в 500 г 2% раствора:
100 г раствора содержит 2 г CuCl₂
500 г раствора содержит х г CuCl₂
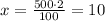 г CuCl₂
г CuCl₂
2) Теперь расчитаем массу раствора 8%, которую нужно будет взять для приготовления 2% раствора (расчитаем массу раствора, в котором будет содержаться 10 г CuCl₂):
100 г раствора содержит 8 г CuCl₂
х г раствора содержит 10 г CuCl₂
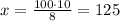 г раствора
г раствора
3) Раз нам дана масса конечного 2% раствора, расчитаем массу воды, которую необходимо добавить к нашему 8% раствору:
m(H₂O)=500-125=375 г
ответ: для приготовления 500 г 2% раствора потребуются 125 г 8% раствора и 375 г воды.
H₂SO₄ + Ba(NO₃)₂ = BaSO₄ + 2HNO₃
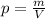 ⇒ m=p×V
⇒ m=p×V
I часть
1) Найдем массу 15%-ного раствора H₂SO₄ и массу 10% раствора Ba(NO₃)₂:
m(H₂SO₄)=1,2×200=240 г
m(Ba(NO₃)₂)=1,04×150=156 г
2) Найдем массу раствора, который образовался после сливания серной кислоты и нитрата бария:
mобщего_раствора=mр-ра(H₂SO₄) +mр-ра(Ba(NO₃)₂)=240+156=396 г.
3) Найдем массы чистых (безводных веществ):
mвещества= ω%×mраствора÷100%
m(H₂SO₄)= 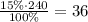 г
г
m(Ba(NO₃)₂)= 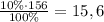 г
г
Как видно, серной кислоты в избытке, поэтому расчет будем вести по нитрату бария.
II часть
В образовавшемся растворе присутствуют осадок BaSO₄ и непрореагировавшая кислота H₂SO₄. Для того, чтобы узнать массовую долю H₂SO₄ в образовавшемся растворе, надо узнать массу осадка BaSO₄ и вычесть ее из массы нового раствора (чтоб осталась масса раствора с H₂SO₄).
1) Найдем массу образовавшегося осадка BaSO₄:
M(Ba(NO₃)₂)=261 г/моль
M(BaSO₄)=233 г/моль
m(Ba(NO₃)₂)=15,6 г
m(BaSO₄)= x г
261 г Ba(NO₃)₂ дают 233 г BaSO₄
15,6 г Ba(NO₃)₂ дают х г BaSO₄
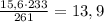 г BaSO₄
г BaSO₄
2) Найдем массу образовавшегося раствора без осадка:
mнов_р-ра= 396-13,9 = 382,1 г
3) Найдем массу H₂SO₄, которая прореагировала с Ba(NO₃)₂: M(Ba(NO₃)₂)=261 г/моль
M(H₂SO₄)=98 г/моль
m(Ba(NO₃)₂)=15,6 г
m(H₂SO₄)= y г
261 г Ba(NO₃)₂ прореагировало с 98 г H₂SO₄
15,6 г Ba(NO₃)₂ прореагировало с у г H₂SO₄
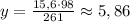 г H₂SO₄
г H₂SO₄
4) Найдем массу оставшейся в новом растворе серной кислоты (безводной) (см. I часть п.3)):
m(H₂SO₄)ост= 36-5,9 = 30,1 г
5) Найдем массовую долю оставшейся кислоты в новом растворе:
ω=m(H₂SO₄)/m(раствора)×100%=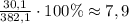
ответ: массовая доля H₂SO₄ в образовавшемся растворе 7,9%.