Во первых определяешь реальное количество натрия в 11,5 г: если 2 % примеси, то 98 % - натрий 11,5*98/100 = 11,27 г уравнением: 2na + 2h2o > 2naoh + h2 м.м. судя по уравнению из 46 г натрия получается 2 г водорода, из 11,27 г - 11,27*2/46 = 0,49 г поскольку выход 95 %, то реально получится 0,49г *95/100 = 0,4655 г при ну моль газа занимает объем 22,4 л. моль - это количество вещества в г, численно равное его м.массе. т.е., для водорода 2 г занимает объем 22,4 л, отсюда выделившийся водород займет 0,4655*22,4/2=5,21 л имей в виду, можно сразу решить в литрах. я объяснила в г, чтобы было более понятно. коэффициенты в уравнениях означают количества молей реагентов и продуктов, т.е. на 2 моля натрия нужно 2 моля воды и образуется 1 моль водорода, вот
Сера: 1s2 2s2 2p6 3s2 3p4 Хром: 1s2 2s2 2p6 3s2 3p6 3d5 4s1На внешнем уровне хрома 1 электрон , остальные 5 его валентных электронов на предпоследнем уровне, поэтому для образования устойчивого состояния s2p6 хрому выгоднее отдать электроны и проявить восстановительные свойства. У серы же все шесть валентных электронов на внешнем уровне и к тому же значительно меньший радиус атома. Для обретения устойчивого состояния s2p6 атому серы выгоднее принять два электрона и проявить окислительные свойства, во всяком случае при взаимодействии с металлами и водородом. Сера принадлежит к р-элементам, хром - к d-элементам. Атомы этих элементов естественно имеют возбужденное состояние. "Провал" электрона у хрома объясняется тем, что состояние d5, когда в каждой из пяти квантовых ячеек d-подуровня по одному электрону более энергетически выгодно, чем состояние d4.
- Электролиз раствора:
K(-):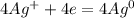
An(+):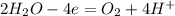
- Рассчитаем массу расворенного вещества соли:
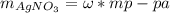 = 900г*0,36 = 324 грамм
= 900г*0,36 = 324 грамм
- Рассчитаем количество вещества соли:
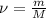 = 324 грамм/170г/моль = 1,9 моль
= 324 грамм/170г/моль = 1,9 моль
- По уравнению реакции:
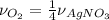 = 1,9моль/4 = 0,476моль
= 1,9моль/4 = 0,476моль
- Рассчитаем массу кислорода:
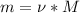 = 0,476моль*32г/моль = 15,232 грамм
= 0,476моль*32г/моль = 15,232 грамм