х г 12 л
106 г 22,4 л
1. Знайдемо чисту масу кальцинованої соди:
при взаємодіїї 106 г соди віділяється 22,4 л вуглекислого газу, а
при -- // -- х г_________________12 л, звідки
х=106*12/22,4=57 г
2. Тепер,віднявши від загальної маси зразка отриману чисту масу соди,отримаємо масу домішків:
m(домішків)=m(зразка) - m(Na2CO3)=68 - 57 =11 г
3. Віднесемо масу домішків до загальної маси зразка і отримаємо масову частку домішків:
w(домішків)=m(домішків)/m(зразка)=11/68=0,16 або 16%
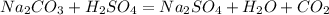
1. Найактивніший неметал V групи - N (нітроген) 2. Елемент з номером 9 - F (флуор). Формула сполуки - HF 3. Це Mg (магній). Формула вищого оксиду - MgO. 4. Дано: Mr(R2O3) = 70 Mr (R2O3) = 70 R - ? Mr (R2) = Mr (R2O3) - Mr (O3)
Mr (R2) = 70 - 48 = 22
Ar (R) = Mr (R2)/2
Ar (R) = 22/2 = 11
R - B (бор)
Відповідь: R - B (бор)