Водородный показатель (рН) величина, характеризующая активность или концентрацию ионов водорода в растворах. Водородный показатель обозначается рН.
Водородный показатель численно равен отрицательному десятичному логарифму активности или концентрации ионов водорода, выраженной в молях на литр:
pH=-lg[ H+ ]
В воде концентрация ионов водорода определяется электролитической диссоциацией воды по уравнению
H2O=H++OH-
Константа диссоциации при 22° С составляет
Пренебрегая незначительной долей распавшихся молекул, можно концентрацию недиссоциированной части воды принять равной обшей концентрации воды, которая составляет: С[H2O ]=1000/18=55,55моль/л.
Тогда:
C[ H+ ] ·C[ OH- ]=K·C[H2O]=1,8·10-16·55,55=10-14
Для воды и ее растворов произведение концентраций ионов Н+ и ОН- величина постоянная при данной температуре. Она называется ионным произведением воды КВ и при 25° С составляет 10-14.
Постоянство ионного произведения воды дает возможность вычислить концентрацию ионов H+если известна концентрация ионов OH-
и наоборот:
Понятия кислая, нейтральная и щелочная среда приобретают количественный смысл.
В случае, если [ H+ ] =[ OH- ]эти концентрации (каждая из них) равны моль/л, т.е [ H+ ] =[ OH- ]=10-7моль/л и среда нейтральная, в этих растворах
pH=-lg[ H+ ]=7 и рОН=-lg[ OH-]=7
Если [ H+ ]>10-7моль/л, [ OH-]<10-7моль/л -среда кислая; рН<7.
Если [ H+ ]<10-7 моль/л, [ OH-]>10-7моль/л -среда щелочная; рН>7.
В любом водном растворе рН + рОН =14, где рОН=-lg[ OH-]
Величина рН имеет большое значение для биохимических процессов, для различных производственных процессов, при изучении свойств природных вод и возможности их применения и т.д.
▶Качественной реакцией на сульфит-ионы 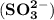 является выделение бесцветного газа с резким запахом - оксида серы (Ⅳ)
является выделение бесцветного газа с резким запахом - оксида серы (Ⅳ) 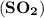 при добавлении в раствор сильной кислоты (например,
при добавлении в раствор сильной кислоты (например, 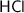 ).
).
 - молекулярное уравнение.
- молекулярное уравнение.
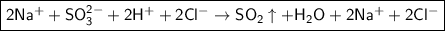 - полное ионное уравнение.
- полное ионное уравнение.
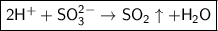 - сокращённое ионное уравнение.
- сокращённое ионное уравнение.
▷Признак реакции - выделение бесцветного газа с резким запахом - 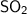 .
.
Качественной реакцией на сульфид-ионы 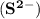 является выделение бесцветного газа с неприятным запахом - сероводорода
является выделение бесцветного газа с неприятным запахом - сероводорода 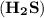 при добавлении в раствор сильной кислоты (например,
при добавлении в раствор сильной кислоты (например, 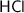 ).
).
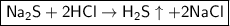 - молекулярное уравнение.
- молекулярное уравнение.
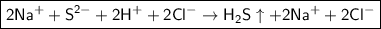 - полное ионное уравнение.
- полное ионное уравнение.
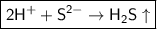 - сокращённое ионное уравнение.
- сокращённое ионное уравнение.
▷Признак реакции - выделение бесцветного газа с неприятным запахом - 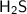 .
.
Итак, если при добавлении соляной кислоты в одну из пробирок выделяется газ с запахом жжённых спичек - 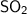 , то это значит, что в растворе содержится сульфит натрия -
, то это значит, что в растворе содержится сульфит натрия - 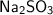 . Если при добавлении соляной кислоты в одну из пробирок выделяется газ с запахом тухлых яиц -
. Если при добавлении соляной кислоты в одну из пробирок выделяется газ с запахом тухлых яиц - 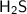 , то это значит, что в растворе содержится сульфид натрия -
, то это значит, что в растворе содержится сульфид натрия - 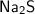 .
.