1. Если 1000 мл воды содержит 200 мг гидрокарбоната, то
250 мл________________х мг, откуда х=250*200/1000=50 мг или 0,05 г
0,05 г х г
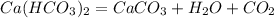
162 г 100 г
При разложении 162 г гидрокарбоната выпадает 100 г карбоната, а
при -- // -- 0,05 г_______________________у г, откуда
у=0,05*100/162=0,03 г или 30 мг
2. Примем массу гидроксида за Х, подставим в формулу по определению массовой доли растворенного вещества и получим уравнение:
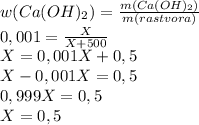 г
г
Теперь,подставив в уравнение массу гидроксида,определим массу оксида:
у г 0,5 г
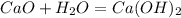
56 г 74 г
при взаимодействии 56 г оксида образуется 74 г гидроксида, а
при -- // -- у г_________________0,5 г, откуда
у=56*0,5/74=0,38 г
1. Если 1000 мл воды содержит 200 мг гидрокарбоната, то
250 мл________________х мг, откуда х=250*200/1000=50 мг или 0,05 г
0,05 г х г
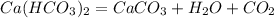
162 г 100 г
При разложении 162 г гидрокарбоната выпадает 100 г карбоната, а
при -- // -- 0,05 г_______________________у г, откуда
у=0,05*100/162=0,03 г или 30 мг
2. Примем массу гидроксида за Х, подставим в формулу по определению массовой доли растворенного вещества и получим уравнение:
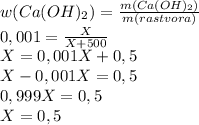 г
г
Теперь,подставив в уравнение массу гидроксида,определим массу оксида:
у г 0,5 г
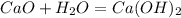
56 г 74 г
при взаимодействии 56 г оксида образуется 74 г гидроксида, а
при -- // -- у г_________________0,5 г, откуда
у=56*0,5/74=0,38 г
m(латуні) = 6,5 г
V(H2) = 0,896 л
m(Zn)-?
m(Cu)-?
ω(Zn)-?
ω(Cu)-?
Розв'язування.
M(Zn)=65 г/моль
M(Cu)=64 г/моль
Vm=22,4 л/моль
n(H2)=V(H2)/Vm
n(H2)=0.896 л/22,4 л/моль=0,04 моль
З хлоридною кислотою буде реагувати тільки цинк, тобто визначаємо масу цинка.
Zn + 2HCl = ZnCl2+H2↑
Зі стехіометричних коефіцієнтів рівняння реакції слідує, що
n(Zn)=n(H2) = 0,04 моль
m(Zn) = n(Zn)×M(Zn) = 0,04 моль×65 г/моль=2,6 г
m(Cu) = m(латуні)-m(Zn)
m(Cu)=6,5 г-2,6 г=3,9 г
ω=m/m(латуні)
ω(Zn)=2,6 г/6,5 г = 0,4 = 40%
ω(Сu) = 3.9 г/6,5 г = 0,6 = 60%
Відповідь: До складу латуні масою 6,5 г входять 2,6 г цинку та 3,9 г міді, що у відсотковому співвідношенні складає відповідно 40% та 60%.