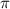 : p = сRT ,
: p = сRT , 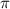 прямо пропорционально молярной концентрации раствора с и температуре Т. Осмотическое давление равно давлению, которое производило бы растворенное вещество, если бы оно в виде идеального газа занимало тот же объем, что и в растворе при той же температуре. Раствор, содержащий 1 моль растворенного вещества в 22,4 л, имеет при 0 градусов осмотическое давление, равное 1 атм. Зная осмотическое давление, можно вычислить молярную массу растворенного вещества М2 в разбавленном растворе.
прямо пропорционально молярной концентрации раствора с и температуре Т. Осмотическое давление равно давлению, которое производило бы растворенное вещество, если бы оно в виде идеального газа занимало тот же объем, что и в растворе при той же температуре. Раствор, содержащий 1 моль растворенного вещества в 22,4 л, имеет при 0 градусов осмотическое давление, равное 1 атм. Зная осмотическое давление, можно вычислить молярную массу растворенного вещества М2 в разбавленном растворе.
заряд ядра атома: +6
IV группа главная подгруппа, 2 малый период, 2 ряд.
¹²С(6р, 6e, 6n)
Ar(C) = 12
электронная конфигурация: 1s² 2s² 2p²
неметалл
высший оксид: CO₂ (кислотные св-ва)
кислородное соединение: H₂CO₃ (кислотные св-ва)
высшее летучее водородное соединение: CH₄
CO₂ + H₂O = H₂CO₃
CO₂ + 2NaOH = Na₂CO₃ + H₂O
CO₂ + HCl=\\
H₂CO₃ + 2NaOH = Na₂CO₃ + H₂O
H₂CO₃ + SO₃ = \\
С имеет более ярко проявляющиеся св-ва, чем кремний.
Углерод имеет менее проявляющиеся металлические св-ва, чем бор и менее проявляющиеся неметаллические св-ва, чем азот.