Химические свойства. Этан вступает в типичные реакции алканов, прежде всего реакции замещения, проходящие по свободнорадикальному механизму. Среди химических свойства этана можно выделить: термическое дегидрирование при 550-650 °C с образованием этилена;
Галогенирование этана проходит поэтапно – за один этап замещается не более одного атома водорода.
Разложение этана (и метана) проводят при температуре больше 1200 градусов: C2H6 ---> 3H2 + 2C. Кстати, именно так промышленным получают высококачественную сажу, необходимую для производства "чёрной" (автомобильной) резины.
Окисление этана. Этан – слабополярное соединение, поэтому при обычных условиях он не окисляется даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.)
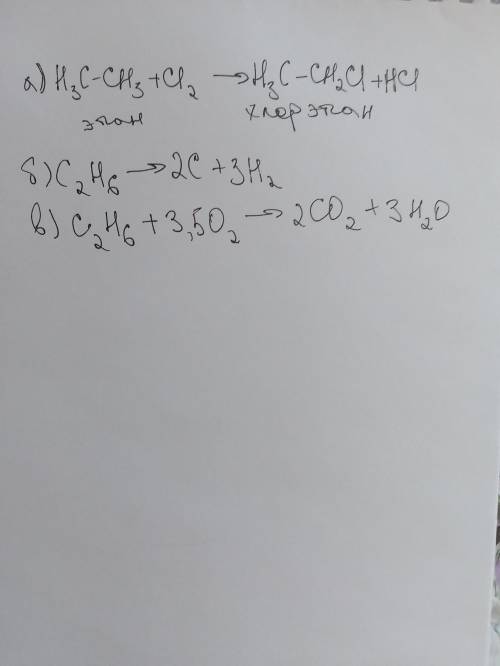
1) Сверху атомная масса
Количество нейтронов = атомная масса - порядковый номер (количество протонов)
а) ⁴He
Количество протонов = 2
Количество нейтронов = 4-2 = 2
б) ²⁴Mg
Количество протонов = 12
Количество нейтронов = 24-12 = 12
в)³⁷Cl
Количество протонов = 17
Количество нейтронов = 37-17 = 20
г)³¹P
Количество протонов = 15
Количество нейтронов = 31-15 = 16
д) ²⁰⁹Bi
Количество протонов = 83
Количество нейтронов = 209-83 = 126
2) Количество вещества = масса вещества / молярная масса вещества
а) Количество вещества (фторид лития LiF) =
= 100г / (7+19)г/моль = 3,85 моль
б) Количество вещества (оксид кремния (IV) SiO₂) =
= 100г / (28+16*2)г/моль = 1,67 моль
в) Количество вещества (бромоводород HBr) =
= 100г / (1+80)г/моль = 1,23 моль