Уравнение реакции( один из вариантов):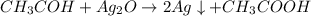
Чтобы расчитать выход продукта, нам нужно узнать сколько теоретически должно было выделиться продукта( "на бумаге").
Воспользуемся известной массой уксусного альдегида и найдём, сколько этого самого альдегида вступило в реакцию:
n( количество вещества) = m( масса) / M( молярная масса) - общая формула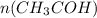 = 4,4 / 44= 0,1 моль
= 4,4 / 44= 0,1 моль
Из уравнения реакции видно, что коэффициент перед уксусным альдегидом равен коэффициенту перед уксусной кислотой, т.е. 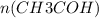 =
= 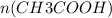 = 0,1 моль
= 0,1 моль
Теперь, пользуясь уже знакомой формулой n( количество вещества) = m( масса) / M( молярная масса), мы можем найти массу ( теоретическую) уксусной кислоты: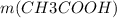 =
= 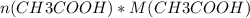 = 0,1 * 60 = 6 г.
= 0,1 * 60 = 6 г.
Выход продукта расчитываем по формуле:
w = m( практ) / m( теор) * 100% = 90%
ответ: выход продукта составил 90%.
ответ:электронные уравнения -
Коэффициенты определяют методом электронного баланса с электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях.
Как правильно составлять электронные уравнения?
1. Запишите схему реакции с указанием исходных и образующихся веществ, определите элементы, которые изменяют в результате реакции степень окисления, найдите окислитель и восстановитель.
2. Составьте электронные уравнения исходя из того, что окислитель принимает электроны, а восстановитель их отдает.
3. Подберите множители (основные коэффициенты) для электронных уравнений так, чтобы число электронов, отданных при окислении, было равно числу электронов, полученных при восстановлении.
4. Расставьте коэффициенты в уравнении реакции.