BA(OH)
NA(OH)
HF
H2SiO3
K(OH )
ZN(OH)
HCl
H2CO3
98,4 г х л
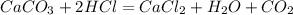
100 г 22,4 л
1.Сначала найдем чистую массу карбоната кальция в мраморе,зная,что в последнем содержится 18% примесей:
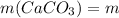 (мрамора)
(мрамора)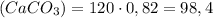 г
г
2. Теперь,подставив эту массу в уравнение реакции,определим объем углекислого газа:
При взаимодействии 100 г карбоната выделяется 22,4 л углекислого газа, а
при -- // -- 98,4 г___________________х л, откуда
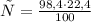 =22,04 л
=22,04 л
Для того чтобы получить нитрат кальция к азотной кислоте можно прибавить кальций или гидроксид кальция(без разницы):
2HNO3 + Ca=Ca(NO3)2 + H2
Для начала найдем массу вещества азотной кислоты, для этого умножим массу раствора на массовую долю:
m(вещества)=200*0,063=12,6 г
Затем узнаем количество азотной кислоты, для этого массу вещества делим на молярную массу азотной кислоты:
n(HNO3)=12,6/63=0,2 моль
Для того чтобы найти выход продукта, нужно знать теоретическую массу, ее мы находим умножив количество нитрата кальция на его молярну массу(количество будет в 2 раза меньше, по коэффициентам в уравнении:
m(теоретическая)=0,1*164=16,4 г
Чтобы узнать выход надо практическую массу поделить на теоретическую:
ω=15/16,4*100%=91,5%
гидроксид бария-Ba(OH)2
едкий натр-NaOH
плавиковая кислота-HF
едкое кали-KOH
гидроксид цинка-Zn(OH)2
соляная кислота-HCl
угольная кислота-H2CO3