K2SO4 - сульфат калия
Ba(NO3)2 - нитрат бария
Na2CO3 - карбонат натрия
Ca3(PO4)2 - фосфат кальция
ZnSO4 - сульфат цинка
FeS - сульфид железа (II)
CuCl2 - хлорид меди (II)
K2SiO3 - силикат калия
Na2SO3 - сульфит натрия
AlBr3 - бромид алюминия
KI - иодид калия
BaCl2 - хлорид бария
ZnSO4 - сульфат цинка
AgNO3 - нитрат серебра
MgCO3 - карбонат магния
Ba(NO3)2 - нитрит бария
Fe2S3 - сульфид железа (III)
В данном списке есть две киcлоты:
H2SiO3 – кремниевая кислота
H3PO4 – фосфорная кислота
И два оксида:
CuO - оксид меди (II)
Al2O3 - оксид алюминия
Объяснение:
Объяснение:
Высший оксид вида
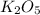
характерен для элементов
V группы а-подгруппы (N, P, As, Sb, Bi)
в таблице Менделеева
Для этих же элементов характерен гидрид вида:
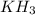
Известно, что в соединении с гидрогеном (водород, Н) массовая доля гидрогена составляет 8.8%.
Напишем уравнение
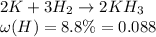
Молекулярная масса КН3 равна:
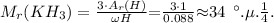
Следовательно, атомная масса элемента К равна:

И действительно в V группе а-подгруппе есть элемент с атомной массой 31 а.е.м.
И этот элемент - фосфор (Р)
Это 15 элемент в Таблице. Его электронная формула имеет вид:
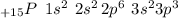
Гидрат оксида фосфора, который соответствует его высшему оксиду (гидроксид фосфора) - это фосфорная кислота, чаще всего имеется в виду ортофосфорная кислота
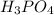
однако может встречаться и метафосфорная кислота
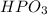
Фосфорная кислота реагирует с
с основными оксидами:
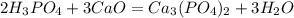
с основаниями:
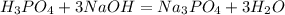
Характерная реакция на фосфат-ионы - взаимодействие с нитратом серебраAgNO3. При этом образуется ярко-желтый осадок фосфата серебра:

Ag¹⁺ + 1e = Ag⁰ - окислитель
H⁰ - 1e = H¹⁺ - восстановитель
Pb²⁺ + 2e = Pb⁰ - окислитель
Na⁰ - 1e = Na¹⁺ - восстановитель
H¹⁺ + 1e = H⁰ - окислитель
Fe³⁺ + 3e = Fe⁰ - окислитель
C⁰ - 4e = C⁴⁺ - восстановитель