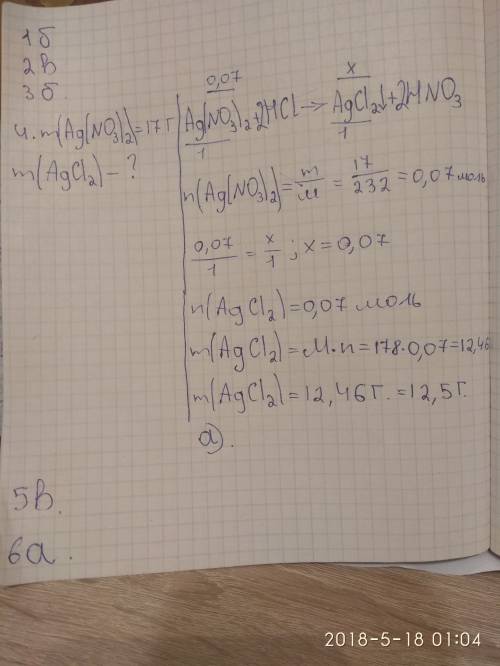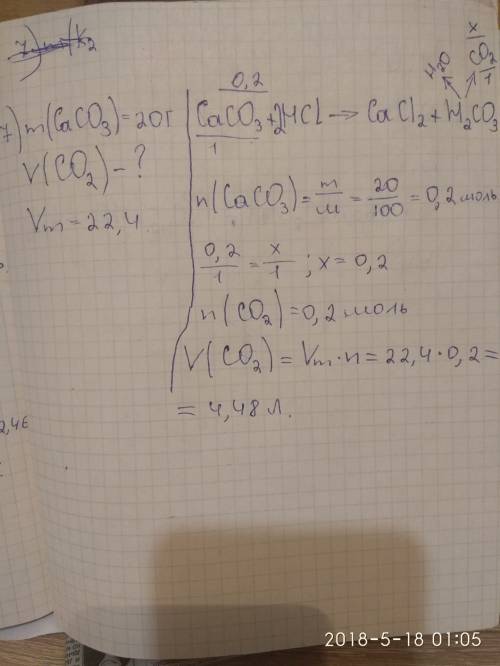1. Укажіть рядок, у якому формула вищого оксиду та його гідрату відповідає елементу з числом протонів 17
А R2O3 та H3RO3 Б RO2 та H2RO3
В RO та R(OH)2 Г R2O7 та HRO4
2. Укажіть атом елемента ІІІ періоду, який в основному стані має максимальне число неспарених електронів
А Фосфор Б Сульфур В Нітроген Г Аргон
3. Укажіть хімічний елемент, який, утворює оксид у вищому ступені окиснення, що має найбільш виражені кислотні властивості
А Силіцій Б Фосфор В Алюміній Г Сульфур
4. Виберіть сучасне формулювання Періодичного закону
А Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від атомної маси
Б Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від атомної ваги
В Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від заряду ядра атома
Г Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від електронегативності
5. Визначте рядок, утворений лише з тих елементів, що входять до головної підгрупи періодичної системи Д.І. Менделєєва
А F; Mn; I Б Li; Na; K
В Al; Ag; S Г Cr; Ca; Hg
6. За електронною формулою атома виберіть елемент, який утворює просту речовину, для якої характерні властивості типового неметалу
А 1s22s22p63s1 Б 1s22s22p63s2
В 1s22s22p63s23р5 Г 1s22s22p63s23p6
7. Укажіть правильне визначення ізотопів
А нукліди одного хімічного елемента
Б нукліди різних хімічних елементів
В прості речовини одного хімічного елемента
Г прості речовини різних хімічних елементів
8. Чому Сульфур і Хром розташовано в одній групі періодичної системи елементів Д.І. Менделєєва
А атоми Сульфуру і Хрому мають однакове число валентних орбіталей
Б атоми Сульфуру і Хрому мають однакове число валентних електронів
В атоми Сульфуру і Хрому мають однакове число енергетичних рівнів
Г Сульфур і Хром мають однакову валентність за Гідрогеном
9. Однакову кількість енергетичних рівнів мають атоми елементів із протонними числами
А 15 і 16 Б 7 і 15 В 8 і 16 Г 15 і 33
10. Визначте число неспарених електронів атома Силіцію в незбудженому стані
А 1 Б 2 В 3 Г 4
11. Визначте протонне число елемента, атом якого на зовнішній електронній оболонці містить два електрони
А 6 Б 20 В 13 Г 16
12. Протій і Дейтерій, що застосовують у атомній енергетиці, є ізотопами атома Гідрогену тому, що це
А прості речовини одного хімічного елемента
Б прості речовини різних хімічних елементів
В нукліди одного хімічного елемента
Г нукліди різних хімічних елементів
13. Однакову кількість електронів на зовнішньому енергетичному рівні мають атоми хімічних елементів з протонними числами
А 6 і 7 Б 13 і 14 В 6 і 14 Г 14 і 22
14. Установіть послідовність зростання окисних властивостей хімічних елементів, які мають таку електронну конфігурацію атомів
А 1s22s22p6 Б 1s22s22p4
В 1s22s22p2 Г 1s22s22p3
15. Установіть послідовність посилення відновних властивостей хімічних елементів, які мають певну електронну конфігурацію атомів
А 1s22s22p63s23p64s1 Б 1s22s1
В 1s22s22p63s1. Г 1s22s22p62s23p63d104s24p64d105s1
16. Розташуйте металічні елементи за зростанням їхньої електронегативності
А Алюміній Б Магній
В Натрій Г Рубідій
17. Розташуйте елементи в ряд за збільшенням числа електронів на зовнішньому енергетичному рівні
А алюміній Б кальцій
В натрій Г силіцій
18. Води лікувальних мінеральних джерел містять практично всі хімічні елементи періодичної таблиці Д. І. Менделєєва. Кількість деяких із них є незначною, це мікроелементи. Установіть відповідність між назвами мікроелементів та електронними формулами їхніх атомів.
Назви мікроелементів
1 Літій
2 Купрум
3 Ферум
4 Флуор
Електронні формули атомів
А 1s22s22p63s23p63d64s2
Б 1s22s1
В 1s22s22p2
Г 1s22s22p5
Д 1s22s22p63s23p63d104s1
test-tube-waving-10926401Перевірити відповіді Ви можете тут