37 г 12,5 л, х л у г
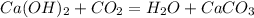
74 г 22,4 г 100 г
1. Визначимо чисту массу гідроксида у розчині:
m(Ca(OH)2)=m(рочину)*w(Ca(OH)2)=50*0,74=37 г
2. Підставивши цю масу до рівняння і прийнявши об'єм вуглекислого газу за Х,визначимо,яка з вихідних речовин прорегує повністю(без залишку):
для повної взаємодії 74 г гідроксида потрібно 22,4 л вуглекислого газу, а
для -- // -- // -- 37 г___________________х л, звідки
х=37*22,4/74=11,2 л
3. Як бачимо,що за умовами вуглекислого газу дано у надлишку,тобто повністю прореагує гідроксид,от за його масою і визначимо масу осаду:
при взаємодії 74 г гідроксиду випадає 100 г осаду, а
при -- // -- 37 г___________________у г, звідки
у=37*100/74=50 г
4Mg + 5H2SO4(конц) = 4MgSO4 + H2S + 4H2O
Mg + SnCl2 = MgCl2 + Sn
Fe + Mn(NO3)2 - реакция не пойдет, т.к железо менее активный металл, чем Mn
Cu + 2AgNO3 = 2Ag + Cu(NO3)2
Hg + ZnSO4 - реакция не пойдет
BaCO3 + 2HNO3 = Ba(NO3)2 + CO2 + H2O
3MgCl2 + 2K3PO4 = Mg3(PO4)2 + 6KCl
NaCl + K2CO3 - реакция не пойдет
Al2(SO4)3 + 6NaOH = 2Al(OH)3 + 3Na2SO4
BaCl2 + CuO - реакция не пойдет