1. a) CaO,
в) 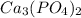
б) HCl
г) 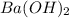
д) 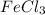
2. Азотная кислота, оксид алюминия (3), гидроксид кальция, сульфат магния, ортофосфорная кислота
3. 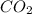 , MgO,
, MgO, 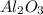 ,
, 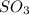 ,
, 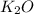
4. В первом +3(промежуточная), во втором -3(низшая), в третьем +5(высшая), в четвертом +2(промежуточная).
5. Решим простую математическую задачу: 200л(полный объем воздуха) * 21%(о,21) = 42 л кислорода
6. Найдём массу1 сахара = о,2 * 80 = 16 кг
найдем массу сахара2 = 16 + 15 = 31 кг
найдем массу раствора2 = 80 + 15 = 95 кг
И новая массовая доля равна: 31/95 * 100% (масса вещества/массу раствора) = 32,63 % или 33%
N+5 + 1e=N+4(окислитель)
O0 +4e=O-2 (окислитель)
N3- - 7e=N+4(восстановитель) *4
Я не уверен что такая реакция возможна
Возможные реакции разложения
NH4NO3= N2O+ 2H2O ОВР : Восстановление:N5+ + 4e− = N+
Окисление:N3− − 4e− = N+
N5+ + N3− = 2N+
2NH4NO3= N2+2NO+ 4H2O
Восстановитель:N3- - 3e− = N
Окислитель:N5+ + 3e− = N+