Аллотропные модификации фосфора
Физические свойства
Фосфор может существовать в виде большого числа аллотропных модификаций, в настоящее время их насчитывается 11, но все многообразие видов можно свести к трем: белый, красный и черный фосфор.
Наиболее распространен белый, или желтый, фосфор. Белый фосфор имеет молекулярную решетку, в узлах которой находятся тетраэдрические молекулы Р4

Ромбическая модификация
Существуют также кубическая и гексагональная модификация.

Кубическая модификация



Гексагональная модификация
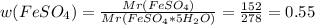 Нашли, что дальше?
Нашли, что дальше?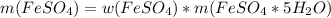 = 0,55*3,5 г.
= 0,55*3,5 г.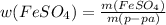 = 1,9г/43,5г = 0,0439 или 4,39% примерно 4,4%
= 1,9г/43,5г = 0,0439 или 4,39% примерно 4,4%
0,42 - 0,01 моль
х-1 моль х=42 г/моль ответ С
х моль 6,62г
2) С6H5OH+3Br2=C6H2OHBr3+3HBr
1 моль 331г/моль
количество фенола 0,02 моль, масса 0,02*94=1,88г ответ С
3) 225г хл
С6Н12О6=2С2Н5ОН + 2СО2
180//моль 44,8л
х=56л ответ Д
4) 4*0,8=3,2 кг чистого СаС2
3,2 кг хм.куб
СаС2+2Н2О=С2Н2+Са(ОН)2
64г/моль 22,4л
х=1,12 м.куб ответ В