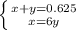
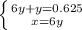
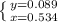
если не правильно что то извините
1. Атомы с одинаковым числом протонов в ядрах ,но разной массой
2. щелочные металлы
3. нейтроны и протоны
4.36 п и 44н
5.количество нейтронов
6.указывает количество энергетических уровней
7.указывает порядковый номер
8.11
9.16
10.16 о 17 о 18 о
11.16
12.39
13.40
14. 8 п и 9 н
15.19 п и 21 н
16.37 п и 17 н
17.3
18.4 и 5
19.53 и 74
20.30 и 35
21.кислоты
22.смесь газов главным образом азота и кислорода
23.уборка улиц
24.азот
25.только 1
26.
27.не выделяет кислород в огонь
28.
29.атомы стали другими атомами
30.А
1. Хим. свойства спиртов:
спирты проявляют как кислотные так и основные свойства,
Кислотные свойства:
Спирты реагируют с щелочными металлами и растворами щелочей
с образованием алкоголят:
R-OH + Na = R-ONa + H2
R-OH + NaOH = R-ONa + H2O
Однако вообще кислотные свойства спиртов мало проявляются, ибо те алкоголяты что получились практически сразу гидролизуются .
Основные свойства:
R-OH + HCl = R-Cl + H2O
Группа OH замещается на галоген .
Спирты окисляются при горении образуя CO2 и H2O (как и обычные углеводороды) .
Спирты могут в присутствии катализаторов Ni/Pt и нагревании дегидрироватся , разделяют дегидрирование на 2 вида:
Внутримолекулярная:
R-OH(Ni, t > 140*C) = CnH2n + H2O (алкен + вода)
Межмолекулярная:
R-OH(Ni, t < 140*C) = CnH2n+2O + H2O (простой эфир + вода)
получения спиртов:
Гидрирование альдегидов либо кетонов, при гидрировании альдегидов получаем первичные спирты, при гидрировании кетонов - вторичные.
Алкен + вода (гидратация алкенов) .
Так-же для отдельных спиртов:
Брожение глюкозы при котором получаем этиловый спирт.
Получение метилового спирта из синтез-газа (CO+H2)
3. Хим.свойства фенолов:
Они почти такие же как и спирты, разве что кислотные свойства ярче выражены, например так-же при реакции с щелочными металлами и щелочными растворами образуются феноляты + водород либо вода .
4. Из альдегидов при гидрировании получают первичные спирты, при гидратации - вещества которые называют гидраты, они существуют при низкой температуре , так-же из них получают полуацетали присоединением спиртов, это тоже типа вещества существующие при низкой температуре. При жёстком окислении из них получают карбоновые кислоты . При реакции с галогенами - получают лекарственные вещества (к примеру тот же хлорат) .
5. Непонятное условие, абсолютно несвязанная информация.
V(NO+N2O) = 14 л
m(O)=m(N)
Найти:
V(NO)-?
V(N2O)-?
Примем кол-во в-ва NO за х моль, а N2O - за у моль
n(NO+N2O) = 14 л/22,4 л/моль = 0,625 моль
х+у = 0,625
14х+28у=16х+16у
Решив систему, получим
х=n(NO) = 0,536 моль
y=n(N2O) = 0,089 моль
V(NO) = 0,536 моль*22,4 л/моль = 12 л
V(N2O) = 0.089 моль*22,4 л/моль = 2 л
ответ: 12 л NO и 2 л N2O