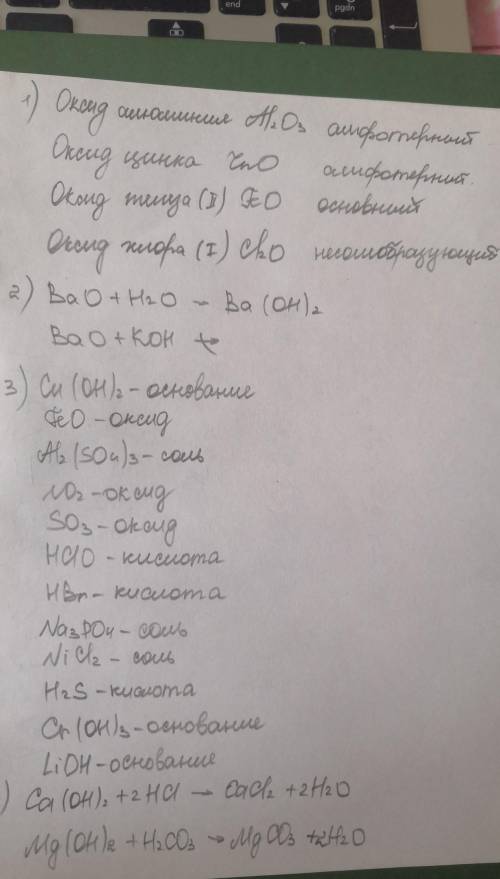Объяснение:
Химические свойства кислот.
Разбавленная серная кислота относится к кислотам-неокислителям и реагирует
а) с металлами стоящими в ряду напряжений до водорода
Mg + H2SO4 = MgSO4 + H2↑
б) с основными оксидами
FeO + H2SO4 = FeSO4 + H2O
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
в) с растворимыми и нерастворимыми основаниями
2KOH + H2SO4 = K2SO4 + 2 H2O
сульфат калия
Если кислота взята в избытке а основание в недостатке, образуются кислые соли:
KOH + H2SO4 = KНSO4
гидросульфат калия
Если кислота реагирует с многокислотным основанием, взятым в избытке, то образуются основные соли:
Al(OH)3 + H2SO4 = (AlOH)SO4 + 2 H2O
гидроксосульфат алюминия
в) некоторыми солями
Наиболее разнообразны реакции кислот с солями. При взаимодействии кислоты и соли (если эта реакция происходит) образуются новая кислота и новая соль.
Эти реакции идут до конца если:
а) один один из продуктов реакции -либо соль, либо кислота - оказывается малорастворимыми и выпадают в осадок.
Рассмотрим примеры
Н2SO4 + BaCl2 = BaSO4↓ + 2HCl
Н2SO4 + K2SiO3 = K2SO4 + H2SiO3↓
б) один из продуктов реакции выделяется в виде газа
Н2SO4 + Na2S = Na2SO4 + H2S↑
в) Кислота может реагировать и с нерастворимыми солями. Это возможно обычно в том случае если кислота более сильная и вытеснить более слабую или более летучую кислоту из раствора её соли или из твердой соли
Ca3(PO4)2 (тв) + 3H2SO4 = 3CaSO4 ↓ + 2H3PO4
СаСl2 (p-p) + H2SO4 = CaSO4↓ + 2HCl
г) в том случае если новая кислота и новая соль находятся в растворе, то такие реакции не идут до конца и обратимы:
Сu(NO3)2 p-p + H2SO4 p-p ⇄ CuSO4 p-p + 2HNO3 p-p
1) Оксид бария BaO основный оксид
Оксид алюминия Al2O3 амфотерный оксид
Оксид селена(4) SeO2 кислотный оксид
Оксид хрома(6) CrO3 кисотныц оксид
2) SO2+H2O➡️H2SO3
SO2+HCl не идёт
3)CuSO4 соль
Fe(OH) 2 основание
Al2O3 оксид
СО2 оксид
ВаSO4 соль
Cl2O7 оксид
HBR кислота
H3РO4 кислота
Ni(OH) 2 основание
H2SO3 кислота
Na2SO3 соль
LIOH основание
4)H2SO4+2KOH➡️K2SO4+2H2O
2HNO3+Ba(OH)2➡️Ba(NO3)2+2H2O
5) по растворимости
Основания Mg(OH)2, Pb(OH) 2, Al(OH)3
Щелочи CsOH , KOH, Ba(OH)2
6)Сульфид калия K2S
Сульфид железа(3) Fe2S3
Сульфид стронция SrS
Хлорид калия KCl
Хлорид железа (3) FeCl3
Хлорил стронция SrCl2
Нитрат калия KNO3
Нитрат железа (3) Fe(NO3) 3
Нитрат стронция Sr(NO3)2
4Li+O2➡️2Li2O
Li2O+H2O➡️2LiOH
LiOH+HNO3➡️LiNO3+Н2О
4V+5O2➡️2V2O5
n(V2O5) =50/182=0.27 молт
5-----------2
0.27----x
X=0.108 моль
m(V) =0.108*51=5.508 г
Второй вариант в фото