
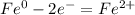
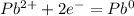
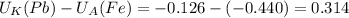 В (Вольт)
В (Вольт)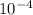 то ЭДС необходимо рассчитать с формулы Нернста:
то ЭДС необходимо рассчитать с формулы Нернста:![((U_{K})^o+ \frac{0,059}{n}lg[Me^{n+}]_k)-( (U_{A})^o)+ \frac{0,059}{n}lg[Me^{n+}]_a )](/tpl/images/0408/4708/bd0bf.png)
 В (Вольт)
В (Вольт).
.
.
.
.
.
.
.
.
§¥₩£$₽§:-)∆№{{<∆ $√∆ <£:-)∆]{:-)£|°:-)£÷∆ـ÷£:-)∆]°:-)]°°ـ∆]÷∆ £÷°:-)£÷°]÷°:-)£÷°:-)°÷£ـ°<£:-)÷°§°÷°ـ°÷°ـ]°:-)∆]∆ـ∆÷∆:-)∆§∆]{ ∆]∆:-)∆<°ـ÷£:-)°√2:-)°|3ـ]°÷2:-)£÷°÷:-)£÷∆3]°]:-)2÷°ـ°÷£ـ÷°:-)3|{ـ{÷£ـ£]:-){]{]°]¥:-)÷£:-)£<°§£<£§£<§°§°]§°<£§<°§£]°:-)|°:-)]£°:-)÷°:-)£]£]÷£:-)£÷£]°÷]°÷£<£÷÷£]°£÷]£]£]£÷$:-)°÷£]£÷£ـ£]£]
Объяснение:
> °<°] °÷°] ÷°°:-) ÷°] ÷£:-) °√∆÷:-) £] °] $÷ـ°÷°:-) ÷£:-) °÷<£√<°÷°2√<2:-)°] ∆÷£:-) ∆÷£:-) ∆:-) ∆£÷§°÷№] £÷°§∆÷§£÷£]{÷÷£°:-)] °] °<°<°
w/об.(N₂)=78,1%
w/об.(O₂)=20,9%
w/об/(Ar)=1,0%
объем азота до и после взрыва
v(N₂)=v*w/об.(N₂)
v(N₂)=130*0,781=101,53 мл
объем кислорода до взрыва
v(O₂)=v*w/об.(O₂)
v(O₂)=130*0,209=27,17 мл
объем аргона до и после взрыва
v(Ar)=v-v(N₂)=v(O₂)
v(Ar)=1,30 мл
C₃H₈ + 5O₂ = 3CO₂ + 4H₂O
C₃H₈ : O₂ = 1:5
5 : 27,17 = 1 : 5,434 пропан в недостатке по схеме реакции
объем углекислого газа после взрыва
v(CO₂)=3v(C₃H₈)
v(CO₂)=15 мл
объем паров воды после взрыва
v(H₂O)=4v(C₃H₈)
v(H₂O)=20 мл
объем кислорода после взрыва
Δv(O₂)=v(O₂)-5v(C₃H₈)
Δv(O₂)=27,17-25=2,17 мл
итого после взрыва:
v(N₂)=101,53 мл
Δv(O₂)=2,17 мл
v(Ar)=1,30 мл
v(CO₂)=15 мл
v(H₂O)=20 мл