3) По уравнению n = n(NaOH) / 2 = 0,125 моль / 2 = 0,0625;
4) m = n * M = 0,0625 * 97 г/моль = 6,0625 г.
ответ: m = 6,0625 г.
Абсолютно уверен, что у меня решено верно! Это задача простая! Никакого избытка с недостатком нет!
------------------------------------------------------------------------------------------------- Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."
Нам дано 180 г 5% р-ра NaOH. В этом растворе масса гидроксида натрия составит: m(NaOH)= 180 r*0.05 = 9 r При добавлении к раствору 6,9 г натрия произойдет реакция его с водой. Рассчитаем массу образовавшегося гидроксида натрия. M(Na) = 23 г/моль n(Na)=m/M = 6,9 г/23 г/моль = 0,3 моль 2Na + 2H2O = 2NaOH + H2↑ Из уравнения реакции видим, что n(NaOH)=n(Na) n(NaOH)=0.3 моль Находим массу образовавшегося в ходе реакции NaOH: M(NaOH)=40 г/моль m'(NaOH) = 0,3 моль*40 г/моль = 12 г Находим массу выделившегося водорода, из уравнения реакции следует, что его количество вдвое меньше натрия. n(H2) = 0,15 моль М(Н2) = 2 г/моль m(H2) = n*M = 0.15 моль*2 г/моль = 0,3 г Рассчитываем массы раствора и гидроксида натрия: m"(p-pa NaOH) = 180 г + 6,9 г - 0,3 г = 186,6 г m"(NaOH)= 9 г +12 г = 21 г ω"(NaOH) = 21 г/186,6 г = 0,1125 или 11,25% ответ: 11,25%
Нам дано 180 г 5% р-ра NaOH. В этом растворе масса гидроксида натрия составит: m(NaOH)= 180 r*0.05 = 9 r При добавлении к раствору 6,9 г натрия произойдет реакция его с водой. Рассчитаем массу образовавшегося гидроксида натрия. M(Na) = 23 г/моль n(Na)=m/M = 6,9 г/23 г/моль = 0,3 моль 2Na + 2H2O = 2NaOH + H2↑ Из уравнения реакции видим, что n(NaOH)=n(Na) n(NaOH)=0.3 моль Находим массу образовавшегося в ходе реакции NaOH: M(NaOH)=40 г/моль m'(NaOH) = 0,3 моль*40 г/моль = 12 г Находим массу выделившегося водорода, из уравнения реакции следует, что его количество вдвое меньше натрия. n(H2) = 0,15 моль М(Н2) = 2 г/моль m(H2) = n*M = 0.15 моль*2 г/моль = 0,3 г Рассчитываем массы раствора и гидроксида натрия: m"(p-pa NaOH) = 180 г + 6,9 г - 0,3 г = 186,6 г m"(NaOH)= 9 г +12 г = 21 г ω"(NaOH) = 21 г/186,6 г = 0,1125 или 11,25% ответ: 11,25%
Дано:
mр-ра(NaOH) = 100г.
W (NaOH) = 5%
Найти:
m(Cu(OH)2) - ?
Выпал осадок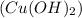
1) mчист.в-ва(NaOH) = mр-ра(NaOH) * W(NaOH) / 100% = 100г. * 5% / 100% = 5г.;
2) n(NaOH) = mчист.в-ва(NaOH) / M(NaOH) = 5г. / 40 г/моль = 0,125 моль;
3) По уравнению n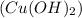 = n(NaOH) / 2 = 0,125 моль / 2 = 0,0625;
= n(NaOH) / 2 = 0,125 моль / 2 = 0,0625;
4) m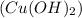 = n
= n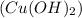 * M
* M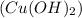 = 0,0625 * 97 г/моль = 6,0625 г.
= 0,0625 * 97 г/моль = 6,0625 г.
ответ: m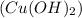 = 6,0625 г.
= 6,0625 г.
Абсолютно уверен, что у меня решено верно! Это задача простая! Никакого избытка с недостатком нет!
-------------------------------------------------------------------------------------------------
Есть вопросы? Задавай Если человек знает, чего он хочет, значит, он или много знает, или мало хочет."